단축키
Prev이전 문서
Next다음 문서
단축키
Prev이전 문서
Next다음 문서
부정적인 임신 결과를 예방하려면 임신 중 비타민 D 보충이 필요할 수 있습니다. 이 리뷰는 2012년에 처음 출판된 후 2016년에 출판된 리뷰의 업데이트입니다.
목표
임신 중 여성에게 비타민 D 보충제를 단독으로 투여하거나 칼슘이나 다른 비타민 및 미네랄과 함께 투여하면 산모와 신생아의 결과를 안전하게 개선할 수 있는지 여부를 조사합니다.
검색방법
이번 업데이트를 위해 우리는 Cochrane Pregnancy and Childbirth's Trials Register(2018년 7월 12일)를 검색하고, 관련 기관에 연락(2018년 5월 15일)하고, Clinicaltrials.gov 및 WHO 국제 임상시험 등록 플랫폼(2018년 7월 12일)에서 검색된 임상시험 및 레지스트리의 참조 목록을 검색했습니다. . 데이터를 추출하기에 충분한 정보가 있는 경우 초록을 포함했습니다.
선정기준
임신 중 여성을 대상으로 비타민 D 단독 또는 다른 미량 영양소와의 병용 보충 효과를 위약 또는 중재 없음과 비교하여 평가하는 무작위 및 준 무작위 시험.
데이터 수집 및 분석
두 명의 검토 저자가 독립적으로 i) 포함 기준에 대한 임상시험의 적격성을 평가하고, ii) 포함된 임상시험에서 데이터를 추출하고, iii) 포함된 임상시험의 비뚤림 위험을 평가했습니다. 근거의 확실성은 GRADE 접근법을 사용하여 평가되었습니다.
주요 결과
30개 임상시험(여성 7,033명)을 포함시켰고, 60개 임상시험은 제외했으며, 6개 임상시험은 진행 중이거나 출판되지 않은 임상시험으로 확인되었으며, 2개 임상시험은 평가를 기다리고 있습니다.
비타민 D 단독 보충 대 위약/무개입
3,725명의 임산부를 대상으로 한 총 22건의 임상시험이 이 비교에 포함되었습니다. 19개 시험은 대부분의 영역에서 비뚤림 위험이 낮거나 중간 정도인 것으로 평가되었으며, 3개 시험은 대부분의 영역에서 비뚤림 위험이 높은 것으로 평가되었습니다. 임신 중 비타민 D만 보충하면 자간전증 (위험비(RR) 0.48, 95% 신뢰구간(CI) 0.30 ~ 0.79; 4건의 임상시험, 여성 499명, 근거 확실성 중간 ) 및 임신성 당뇨병 (RR) 의 위험을 줄일 수 있습니다. 0.51, 95% CI 0.27 ~ 0.97, 4건의 임상시험, 446명의 여성, 중간 정도의 근거 확실성 ); 위약을 투여 받거나 중재를 받지 않은 여성에 비해 저체중(2,500g 미만) (RR 0.55, 95% CI 0.35 ~ 0.87, 5건의 임상시험, 여성 697명, 근거 확실성 중간) 을 출산할 위험을 줄일 수 있습니다 . 비타민 D 보충은 중재가 없거나 위약에 비해 37주 미만의 조산 위험에 거의 또는 전혀 차이가 없을 수 있습니다 (RR 0.66, 95% CI 0.34 ~ 1.30; 7건의 임상시험, 1640명의 여성, 낮은 근거 확실성 ). 산모의 부작용 측면에서 비타민 D 보충은 심각한 산후 출혈의 위험을 줄일 수 있습니다(RR 0.68, 95% CI 0.51 ~ 0.91; 1건의 임상시험, 1134명의 여성, 낮은 근거 확실성 ). 고칼슘혈증 사례는 없었으며(1건의 임상시험, 1134명의 여성, 낮은 근거 확실성) 비타민 D가 신증후군 위험을 증가 또는 감소시키는지 여부가 매우 불확실합니다(RR 0.17, 95% CI 0.01~4.06, 1건의 임상시험) , 135명의 여성, 매우 낮은 근거 확실성 ). 그러나 산모의 이상반응에 대한 일반적인 데이터가 부족하기 때문에 확고한 결론을 내릴 수는 없습니다.
비타민 D 및 칼슘 보충 대 위약/무개입
이 비교에는 1916명의 임산부를 대상으로 한 9건의 임상시험이 포함되었습니다. 3건의 임상시험은 할당 및 눈가림에 대한 비뚤림 위험이 낮은 것으로 평가되었으며, 4건의 임상시험은 비뚤림 위험이 높은 것으로 평가되었으며, 2건의 일부 구성 요소에는 저위험, 고위험 또는 불분명한 위험이 있었습니다. 임신 중 비타민 D와 칼슘을 보충하면 자간전증 의 위험이 줄어들 수 있습니다 (RR 0.50, 95% CI 0.32 ~ 0.78; 4건의 임상시험, 여성 1174명, 근거 확실성 중간 ). 임신성 당뇨병 에 대한 중재 효과는 불확실합니다 (RR 0.33,% CI 0.01 ~ 7.84; 1건의 임상시험, 54명의 여성, 매우 낮은 근거 확실성 ). 위약을 투여 받거나 중재를 받지 않은 여성과 비교하여 저 출생체중(2500g 미만) (RR 0.68, 95% CI 0.10 ~ 4.55; 2건의 임상시험, 110명의 여성, 매우 낮은 근거 확실성 ). 임신 중 비타민 D와 칼슘 보충 은 위약을 받거나 중재를 받지 않은 여성에 비해 37주 미만 조산 의 위험을 증가시킬 수 있습니다 (RR 1.52, 95% CI 1.01 ~ 2.28; 5건의 임상시험, 942명의 여성, 낮은 근거 확실성 ) . 이 비교에서 산모의 부작용 에 대해 보고된 임상시험은 없습니다 .
비타민 D + 칼슘 + 기타 비타민 및 미네랄 보충 대 칼슘 + 기타 비타민 및 미네랄(비타민 D 없음)
이 비교에는 1,300명의 참가자를 대상으로 한 임상시험이 포함되었습니다. 편견의 위험이 낮은 것으로 평가되었습니다. 전자간증은 평가되지 않았습니다. 비타민 D + 기타 영양소 보충은 37주 미만의 조산 위험에 거의 또는 전혀 차이가 없을 수 있습니다 (RR 1.04, 95% CI 0.68 ~ 1.59; 1회 시험, 여성 1298명, 근거 확실성 낮음 ). 또는 저체중 출생(2500g 미만) (RR 1.12, 95% CI 0.82 ~ 1.51; 1회 시험, 1298명의 여성, 낮은 근거 확실성 ). 임신성 당뇨병 (RR 0.42, 95% CI 0.10 ~ 1.73) 또는 산모의 부작용 (고칼슘혈증 사건 없음, 고칼슘뇨증 RR 0.25, 95% CI 0.02 ~ 3.97, 1회 시험, 여성 1298명 )의 위험에 차이가 있는지 여부는 불분명합니다. ,) 두 결과 모두에 대한 근거의 확실성이 매우 낮은 것으로 나타났기 때문입니다.
저자의 결론
우리는 3개의 개별 비교를 통해 30개의 임상시험(7033명의 여성)을 포함했습니다. GRADE 평가는 중간에서 매우 낮음까지 다양했으며 연구 설계의 한계, 부정확성 및 간접적인 점을 기준으로 등급이 하향 조정되었습니다.
임산부에게 비타민 D만을 보충하면 자간전증, 임신성 당뇨병, 저체중아 출산의 위험을 줄이고 심각한 산후 출혈의 위험을 줄일 수 있습니다. 임신 37주 미만의 조산 위험에는 거의 또는 전혀 차이가 없을 수 있습니다. 임산부에게 비타민 D와 칼슘을 보충하면 자간전증의 위험이 줄어들 수 있지만 37주 미만 조산의 위험이 증가할 수 있습니다(이러한 발견은 추가 연구가 필요함). 임산부에게 비타민 D 및 기타 영양소를 보충하면 임신 37주 미만의 조산 또는 저체중(2,500g 미만) 출생의 위험에 거의 또는 전혀 차이가 없을 수 있습니다. 특히 산모의 부작용 위험과 관련하여 임신 중 비타민 D 보충제의 효과를 평가하려면 추가적인 엄격한 고품질 및 대규모 무작위 시험이 필요합니다.
일반 언어 요약
임신 중 비타민 D 보충제는 여성에게 유익합니까, 아니면 해롭습니까?
이슈가 뭐야?
임신 중에 비타민 D 보충제를 단독으로 또는 칼슘이나 다른 비타민 및 미네랄과 함께 섭취하는 것이 산모나 자녀에게 이익이 되는지 아니면 해를 끼치는지는 확실하지 않습니다.
이것이 왜 중요합니까?
비타민 D는 인간의 건강, 특히 뼈, 근육 수축, 신경 전도 및 일반적인 세포 기능에 필수적입니다. 임산부의 낮은 혈중 비타민 D 농도는 임신 합병증과 관련이 있습니다. 임신 합병증을 예방하려면 임신 중 보충을 통한 추가 비타민 D가 필요할 수 있다고 생각됩니다.
검토에서 무엇을 연구했습니까?
이 리뷰는 2012년에 처음 발표되었고 이후 2016년에 업데이트된 리뷰의 업데이트입니다. 이 리뷰는 임신 중 여성을 위한 비타민 D 단독 또는 다른 미량 영양소와 함께 보충하는 효과를 위약 또는 중재 없음과 비교하여 평가했습니다. 복용량, 보충 시작 기간 또는 시간 또는 보충 유형(경구 또는 주사).
우리는 어떤 증거를 찾았나요?
우리는 증거를 검색했고(2018년 7월) 이 업데이트에 포함할 30건의 임상시험(7033명의 여성이 포함됨)을 찾았습니다.
3,725명의 임산부를 대상으로 한 22건의 임상시험에서 나온 증거에 따르면 임신 중 비타민 D만 보충하면 위약이나 중재가 없는 경우에 비해 자간전증, 임신성 당뇨병, 저체중아 출산 위험이 줄어들 수 있으며 효과가 거의 없거나 거의 없을 수 있습니다. 조산 위험에는 차이가 없습니다. 이는 심각한 산후 출혈과 같은 산모의 부작용 위험을 줄일 수 있지만, 이 결과는 예상치 못한 것이며 단일 임상시험을 기반으로 한 것이라는 점에 유의해야 합니다.
1916명의 임산부를 대상으로 한 9건의 임상시험에서 얻은 증거에 따르면 비타민 D와 칼슘을 보충하면 자간전증의 위험은 줄어들지만 조산의 위험은 높아질 수 있습니다. 이러한 약간의 잠재적인 위험은 산전 관리의 일환으로 칼슘 보충을 받는 여성의 경우 고려해야 할 사항입니다.
1,300명의 임산부를 대상으로 한 한 연구의 증거에 따르면 비타민 D와 기타 영양소를 보충하면 평가된 대부분의 결과 위험에 거의 또는 전혀 차이가 없을 수 있습니다.
대부분의 임상시험에서는 산모의 부작용에 대한 데이터가 부족했습니다.
이것은 무엇을 의미 하는가?
임산부에게 비타민 D만 보충하면 자간전증, 임신성 당뇨병, 저체중아 출산 및 심각한 산후 출혈의 위험이 줄어들 수 있습니다. 임신 37주 미만의 조산 위험에는 거의 또는 전혀 차이가 없을 수 있습니다. 임산부에게 비타민 D와 칼슘을 보충하면 자간전증의 위험이 줄어들 수 있지만 37주 미만 조산의 위험이 증가할 수 있습니다(이러한 발견은 추가 연구가 필요함). 임산부에게 비타민 D 및 기타 영양소를 보충하면 조산 또는 저체중(2,500g 미만) 출생 위험에 거의 또는 전혀 차이가 없을 수 있으며 임신성 당뇨병 및 산모의 부작용에 대한 영향은 불분명합니다. 특히 산모의 부작용 위험과 관련하여 임신 중 비타민 D 보충제의 효과를 평가하려면 추가적인 엄격한 고품질 및 대규모 무작위 시험이 필요합니다.
결과 요약
배경
조건에 대한 설명
비타민 D 대사
비타민 D는 주로 햇빛 노출을 통해 생성되는 지용성 비타민으로 생선 간유, 지방이 많은 생선, 버섯, 달걀 노른자, 간과 같은 일부 식품에서만 자연적으로 발견됩니다(Holick 2007a; Holick 2008 ) . . 칼시페롤 이라고 불리는 두 가지 생리학적 활성 형태의 비타민 D가 있습니다 : D 2 및 D 3 . 비타민 D 2 ( 에르고칼시페롤 이라고도 함 )는 식물에서 합성되는 반면, 비타민 D 3 ( 콜레칼시페롤 이라고도 함 )은 자외선 B(UVB) 방사선에 노출되면 인간의 피하에서 7-디히드로콜레칼시페롤로부터 생성됩니다( DeLuca 2004 ). 보충제의 비타민 D는 비타민 D 2 또는 D 3 으로 발견됩니다 . 후자는 비타민 D의 혈청 농도를 높이고 특히 겨울철에 그 수준을 더 오랫동안 유지하는 데 있어서 비타민 D 2 보다 3배 더 효과적일 수 있습니다 . 또한 그 대사산물은 혈장 내 비타민 D 결합 단백질에 대한 탁월한 친화력을 가지고 있습니다( Armas 2004 ; Logan 2013 ; McCullough 2007 ). 비타민 D는 반감기가 짧기 때문에 지속적인 순환 수준을 유지하려면 적절한 비타민 D 섭취가 필요합니다.
D 2 와 D 3 형태 모두 유사한 대사를 공유합니다. 이들은 먼저 간에서 수산화되어 25 하이드록시비타민 D(25(OH)D 또는 칼시디올)를 형성 한 다음 신장에서 다음 반응에 반응하여 1,25 디하이드록실 비타민 D(1,25(OH) 2D 또는 칼시트리올) 로 생성됩니다. 부갑상선 호르몬(PTH) 수치. 칼시트리올은 뼈의 완전성 및 칼슘 항상성을 비롯한 대사 과정에 관여하는 활성 대사산물이 있는 중요한 호르몬 전단계로 간주됩니다( Wagner 2008 ).
비타민 D가 작용하는 주요 부위로는 인간 태아의 피부, 장, 뼈, 부갑상선, 면역체계, 췌장은 물론 소장과 결장 등이 있습니다( Theodoropoulos 2003 ). 또한 비타민 D는 췌장 베타 세포의 비타민 D 수용체에 결합하고 활성화하여 순환 포도당 수준에 반응하여 인슐린 방출을 조절함으로써 혈액 내 포도당의 정상적인 수준을 유지하는 데 도움이 됩니다( Clifton‐Bligh 2008 ; Maghbooli 2008 ; Palomer 2008 ; Xuan 2013 ). 비타민 D는 또한 칼슘 항상성 조절을 통해 포도당 대사에 간접적으로 영향을 미칩니다( Xuan 2013 ).
비타민 D와 칼슘 사이에는 독특한 관계가 있습니다. PTH는 뼈 흡수를 통해 혈액 내 칼슘 농도를 높이는 역할을 하는 반면, 칼시트리올은 PTH를 억제하고 뼈 이외의 공급원에서 혈청 칼슘 농도를 증가시킵니다. 칼시트리올이 있으면 신장과 장의 칼슘과 인의 흡수가 증가되어 칼슘 상태가 개선됩니다.
비타민 D 상태
혈청 칼시디올 또는 25‐하이드록시비타민 D는 피부에서 생성된 비타민 D와 식품 및 보충제에서 얻은 비타민 D의 합계를 반영하므로 비타민 D 상태를 평가하는 데 사용할 수 있습니다( Jones 2008 ). 이 대사산물은 동일한 방법을 사용하더라도 방법과 실험실 간에 큰 차이가 있어 측정하기 어렵습니다. 이는 샘플 전처리 또는 사용된 용매 추출 시스템의 차이로 설명될 수 있습니다( Hollis 2004 ; Lankes 2015 ).
최근 의학 연구소(IOM)는 일반 인구와 임산부 모두에서 혈청 25-하이드록시비타민 D 농도가 50nmol/L(또는 20ng/mL)보다 높은 것으로 적절한 비타민 D 상태를 정의했습니다( IOM 2011 ). 일부 연구자들은 약 80nmol/L(32ng/mL)의 농도가 PTH 수치를 억제하고 칼슘 흡수를 최대화하고 뼈 질량을 최대화하여 뼈 손실, 낙상 및 골절 비율을 감소시키기 때문에 최적이라고 제안합니다( Dawson ‐Hughes 2005 ; Dawson‐Hughes 2008 ). 임신하지 않은 성인에게 제안된 이러한 높은 수치가 임산부에게도 적합한지는 확실하지 않습니다.
비타민 D 상태는 피부 내 생성을 조절하는 요인(예: 피부 색소 침착, 위도, 복장 규정, 계절, 노화, 자외선 차단제 사용 및 대기 오염)과 흡수 또는 대사에 영향을 미치는 요인에 의해 영향을 받습니다(Holick 2007b ; Maghbooli 2007 ). . 멜라닌은 자외선(UV) 광선을 필터링하는 역할을 하여 피부의 비타민 D 생성을 감소시킵니다. 미국의 히스패닉계와 흑인 인구는 멜라닌 함량이 더 높을 수 있으므로 비타민 D 광합성(햇빛 노출로 인한 내인성 합성)이 감소했습니다( Clemens 1982 ). 이는 동일한 지리적 영역에 거주하는 인종 그룹 간의 비타민 D 농도 차이를 설명합니다. ( 브룩 1980 ; Egan 2008 ; Ganji 2012 ; 마츠오카 1991 ; Nesby‐O'Dell 2002 ; Rockell 2005 ). 개인의 피부 사진형은 장기간 동안 거의 또는 전혀 노출되지 않은 후 처음 적당한 수준의 햇빛에 노출된 후 햇볕에 타는 정도와 후속 태닝 정도를 반영합니다( Gilchrest 2008 ). 광형 I과 II는 최소 홍반 용량(MED) 후에 비타민 D 광합성이 빠릅니다. 대조적으로, 프로토타입 VI는 동일한 MED 용량에 따른 비타민 광합성이 거의 없습니다( Clemens 1982) . 위도의 차이도 비타민 D 농도에 영향을 미치는 것으로 나타났으며, 고위도와 저위도 국가의 개인은 비타민 D 수치가 낮습니다. 자외선의 중요성은 여름과 겨울 사이의 비타민 D 농도의 계절적 변화로 더욱 드러납니다. 즉, 겨울에 비해 여름에 비타민 D 농도가 더 높습니다( Holick 2007b ; Levis 2005 ). 비타민 D 대사는 비만인 개인에게도 영향을 미칩니다. 비타민 D는 체지방 저장소에 축적되어 생체 이용률이 떨어지기 때문입니다( Arunabh 2003 ). 최근에는 비만인의 이러한 낮은 비타민 D 상태가 지방량에서 비타민 D의 단순한 부피 희석으로 설명되었으며( Drincic 2012 ), 그 결과 낮은 수준의 25‐하이드록시비타민 D 유병률이 더 높았으며 이러한 현상은 다음과 같은 사람들에게 더 널리 퍼져 있습니다. 과체중 및 비만 개인을 정상 체중 개인과 비교했습니다( Vilarrasa 2007 ; Vimaleswaran 2013 ; Wortsman 2000 ). 같은 맥락에서, 앉아 있는 활동은 햇빛 노출 감소와 연결될 수 있기 때문에 낮은 비타민 D 수치와도 관련이 있습니다( Ohta 2009 ).
비타민 D 결핍 정도
비타민 D 결핍은 전 세계적으로 흔한 건강 문제일 수 있습니다( Bandeira 2006 ; Palacios 2014 ; van Schoor 2011 ). 일년 내내 햇빛에 노출되는 국가에서도 전 세계적으로 유아, 어린이, 청소년, 성인 및 노인의 낮은 비타민 D 상태에 대한 유병률이 높습니다( Palacios 2014 ). 보고된 유병률은 중동, 특히 소녀와 여성에서 가장 높았지만, 대부분의 남미와 아프리카 국가에서는 데이터가 부족합니다.
임신 중에는 혈중 비타민 D 농도가 낮은 경우도 흔합니다. 임산부와 수유 중인 여성을 대상으로 한 17건의 임상시험(미국 2건, 유럽 6건, 아프리카 1건, 아시아 7건, 오세아니아 1건)을 포함한 검토( Palacios 2014 )에서는 낮은 비타민 D 상태(50 미만 농도로 정의됨)의 유병률이 발견되었습니다. nmol/L)은 미국에서 33%, 캐나다에서는 24%입니다. 유럽에서는 낮은 비타민 D 상태의 유병률은 벨기에 45%, 영국 35%, 네덜란드 44%, 스페인 20%, 독일 77%였습니다. 또한, 비타민 D 결핍(30nmol/L 미만 농도로 정의)의 유병률은 벨기에에서 12%, 영국에서 4%, 네덜란드에서 23%였습니다. 아프리카에서 보고된 유일한 연구에서는 탄자니아의 임산부 139명을 대상으로 한 표본에서 낮은 비타민 D 상태의 유병률(1%)이 매우 낮다고 보고했습니다. 아시아에서는 임산부의 비타민 D 결핍 유병률이 매우 높았습니다. 터키 90%, 이란 67%, 파키스탄 72%, 쿠웨이트 70~83%, 인도 96%, 중국 69%였습니다. 비타민 D 결핍 유병률도 터키 50%, 파키스탄 45%, 쿠웨이트 38~41%, 인도 60%로 매우 높았습니다. 호주에서는 임산부의 48%에서 낮은 비타민 D 상태가 발견되었으며, 15%의 임산부에서 비타민 D 결핍이 발견되었습니다.
가장 최근에는 7개국의 13개 임상시험을 포함한 검토에서 비타민 D 결핍 및 부족의 유병률이 39.4%~76.5%에 달하는 것으로 나타났습니다( van der Pligt 2018 ). 그들은 또한 비타민 D 결핍만 보고했으며 중국(100%), 터키(95.6%), 이란(89.4%) 및 파키스탄(89.0%) 여성 사이에서 유병률이 가장 높은 것으로 나타났습니다.
계절적 변화는 임신 중 혈중 비타민 D 농도가 낮아지는 위험을 증가시키며, 여름철에 비해 겨울철에 혈중 비타민 D 농도가 낮아지는 비율이 더 높습니다( Nicolaidou 2006 ; O'Riordan 2008 ). 위도의 차이는 대다수 임산부의 비타민 D 농도에 영향을 미치는 것으로 나타났습니다( Sloka 2009 ).
산모의 비타민 D 상태 및 건강 결과
임신 중 비타민 D 상태는 생애주기의 가장 중요한 단계입니다. 태아는 이 기간 동안 발달을 위해 이 공급원에 전적으로 의존하기 때문입니다. 임신 중 1,25‐디하이드록시비타민 D는 임신 초기에 증가하고 출산할 때까지 계속 증가합니다( Moller 2013 ). 1,25-디하이드록시비타민 D의 이러한 큰 증가는 이용 가능한 25-디하이드록시비타민 D 수준에 의존하는 것으로 보이지만 칼슘 대사와는 무관하며, 이는 1,25-디하이드록시비타민 D의 높은 수준을 허용하는 임신의 독특한 특징입니다( Pludowski 2013a) ). 따라서 임신 중에 증가된 1,25-디하이드록시비타민 D 수준을 유지하려면 25-디하이드록시비타민 D의 수준을 충분히 높게 유지하는 것이 중요합니다. 이러한 수준은 아직 결정되지 않았지만 여러 실험에서 산모의 비타민 D 상태가 태아 및 신생아의 비타민 D 상태와 유의미한 연관이 있고( El Koumi 2013 ; Sachan 2005 ) 산모의 비타민 D 상태가 임신 중 건강 결과와 연관되어 있는 것으로 나타났습니다. 신생아 및 유아 발달. 이러한 연관에 대해서는 아래에서 설명합니다.
임신 중 비타민 D 상태와 고혈압 장애
임신 중 산모의 비타민 D 결핍은 자간전증(임신 20주 후 새로 발병하는 임신성 고혈압 및 단백뇨)의 위험 증가와 관련이 있으며, 이는 산모 및 주산기 이병률 및 사망률 증가와 관련된 상태입니다( Bodnar 2007 ; Holick) 2008 ; Li 2000b ; MacKay 2001 ; Xiong 1999 ). 8건의 임상시험을 포함하는 메타 분석에서는 비타민 D 결핍과 자간전증 위험 사이의 유의미한 연관성이 발견되었으며, 이는 비타민 D 결핍을 25(OH)D 50 nmol/L(20 ng/mL)로 정의한 연구에서 더욱 분명했습니다. 그리고 미국의 경우( Tabesh 2013 ). 마찬가지로, 31건의 시험을 포함한 또 다른 메타 분석에서도 비타민 D 상태가 낮은 임산부의 자간전증 위험이 78% 더 높은 것으로 나타났습니다(교차비(OR) 1.79; 95% 신뢰 구간(CI) 1.25~2.58)( Aghajafari 2013) ). 7개국에서 실시한 13건의 임상시험을 포함한 가장 최근의 체계적 검토에서도 4건의 임상시험 중 3건에서 임신 중 비타민 D 결핍이 자간전증과 관련이 있는 것으로 나타났습니다( van der Pligt 2018 ).
자간전증이 있는 여성은 혈압이 정상인 여성에 비해 25‐히드록시비타민 D의 농도가 더 낮습니다( Diaz 2002 ; Frenkel 1991 ; Halhali 1995 ; Halhali 2000 ; Tolaymat 1994 ). 자간전증이 있는 여성의 요중 칼슘 수치가 낮은 것(저칼슘뇨증)은 낮은 수치의 비타민 D로 인해 장내 칼슘 흡수가 감소했기 때문일 수 있습니다( 8월 1992 ; Halhali 1995 ). 또한 자간전증과 낮은 혈중 비타민 D 농도는 면역 기능 장애, 태반 이식, 비정상적인 혈관 신생, 과도한 염증 및 고혈압을 포함한 생물학적 메커니즘을 통해 직간접적으로 연관되어 있습니다( Bodnar 2007 ; Cardus 2006 ; Evans 2004 ; Hewison 1992 ; Li 2002) ). 비타민 D는 초기 태반 발달에 영향을 미칠 수 있으며, 따라서 유전자 조절 및 발현에서의 역할을 통해 자간전증 발병에 영향을 줄 수 있습니다. 이를 확인하려면 아직 더 많은 연구가 필요합니다.
비타민 D 상태 및 기타 산모 조건
임신 초기의 낮은 혈중 비타민 D 농도는 임신성 당뇨병의 위험 증가와 관련이 있습니다( Farrant 2009 ; Zhang 2008 ). 31개 관찰 실험에 대한 메타 분석에서는 낮은 비타민 D 수치가 임신성 당뇨병 위험을 49% 증가시키는 것으로 나타났습니다(교차비(OR) 1.49; 95% 신뢰 구간(CI) 1.18~1.89)( Aghajafari 2013 ). 24개 관찰 연구에 대한 또 다른 메타 분석에서도 비슷한 결과가 발견되었습니다( Wei 2013 ). 임신 초기에 산모의 당뇨병을 제대로 관리하지 못하는 것은 산모의 낮은 비타민 D 상태와 마찬가지로 유아의 낮은 뼈 미네랄 함량과 역의 상관관계가 있습니다( Namgunga 2003 ). 비타민 D 결핍(VDD)은 신생아 및 유아 VDD 외에도 산모에게 높은 골 교체율, 골 손실, 골연화증(뼈의 연화) 및 근육병증(근육 약화)을 유발할 수 있습니다( El Koumi 2013 ; Glerup 2000 ; Lips 2001) ).
적절한 비타민 D 상태는 또한 다른 불리한 임신 결과로부터 보호할 수도 있습니다. 예를 들어 산모의 비타민 D 결핍은 제왕절개와 연관되어 있지만( Merewood 2009 ; Scholl 2012 ) 관련된 메커니즘은 불분명합니다. 임신 중 비타민 D 결핍이 골반 근육의 힘과 조절력을 감소시킬 수 있다고 제안되었지만( Scholl 2012 ), 이는 확인될 필요가 있습니다.
산전 및 산모의 비타민 D 농도가 낮으면 다른 조직의 기능에 영향을 주어 다발성 경화증, 암, 인슐린 의존성 당뇨병, 나중에 정신분열증의 위험이 커질 수 있습니다( Mcgrath 2001 ).
비타민 D 상태와 조산 및 저체중아 출산
산모의 비타민 D 상태와 조산(임신 기간 37주 미만) 사이의 잠재적인 역 연관성이 보고되었습니다( Dawodu 2011 ; Morley 2006 ). 반대로, 모든 연구에서 산모의 칼시디올 수준과 출생 시 또는 생후 첫 달 동안의 아이 크기 측정 사이에 유의미한 연관성을 보여주는 것은 아닙니다( Bodnar 2010 ; Farrant 2009 ; Gale 2008 ; Morley 2006 ).
24개 관찰 연구에 대한 메타 분석에서는 낮은 비타민 D 수치(< 50nmol/L)와 조산 위험 증가(OR 1.58; 95% CI 1.08~2.31) 사이의 연관성이 확인되었습니다( Wei 2013 ). 또한 두 가지 메타 분석에서는 낮은 비타민 D 상태와 임신 연령에 비해 작은 것 사이의 유의미한 연관성도 발견했습니다( Theodoratou 2014 ; Wei 2013 ). 출생 체중과 관련하여, 3개의 관찰 연구를 포함한 메타 분석에서는 잠재적 교란 요인에 대한 조정 후 산모의 비타민 D 상태와 출생 체중 사이에 약한 긍정적 연관성이 있는 것으로 나타났습니다( Harvey 2014 ). 그러나 4개의 관찰 연구를 포함한 또 다른 메타 분석에서는 이러한 변수( Theodoratou 2014 ). 7개국의 13개 연구를 포함한 가장 최근의 체계적 검토에서는 7개 연구 중 4개에서 임신 중 비타민 D 결핍이 저체중 출생과 관련이 있는 것으로 나타났습니다( van der Pligt 2018 ).
HIV에 감염된 임산부에게서 태어난 아이의 산모 비타민 D 상태와 저체중 출생 또는 조산에 대한 정보는 많지 않습니다( Mehta 2009 ). 연구에 따르면 HIV에 감염된 임산부 사이에서 비타민 D 결핍의 유병률이 높은 것으로 보고되었습니다( Eckard 2013 ; Mave 2012 ).
비타민 D 상태와 출생 후 성장
일부 관찰 연구에서는 임신 중 비타민 D 수치가 태아 뼈 발달과 어린이의 성장에 영향을 미치는 것으로 나타났습니다( Bodnar 2010 ; Brooke 1980 ; Ioannou 2012 ; Mahon 2010 ; Morley 2006 ). 그러나 9개의 관찰 연구에 대한 체계적인 검토에서 밝혀진 바와 같이 산모의 비타민 D 상태와 머리 둘레 사이에는 일관되지 않은 연관성이 있습니다( Harvey 2014 ). 그러나 한 연구에 따르면 9세 어린이의 머리 둘레는 산모의 칼시디올 수치와 유의미한 연관이 있는 것으로 나타났습니다( Gale 2008 ). 산모의 비타민 D 상태와 유아의 골량에 관해서도 일치하지 않는 결과가 있습니다( Akcakus 2006 ; Harvey 2014 ; Javaid 2006 ; Viljakainen 2010 ).
구루병은 일반적으로 아동기 후반에 확인되기 때문에 산모의 비타민 D 결핍이 신생아 구루병으로 이어지는지는 확실하지 않습니다. 초기 연구에서는 골연화증이 있는 여성의 자손에서 신생아 구루병의 위험 가능성, 인, 칼슘 또는 비타민 D 결핍으로 인한 뼈의 비정상적 연화 가능성이 있음을 나타냅니다( Ford 1973 ). 보다 최근의 연구에 따르면 구루병이 있는 아랍 어린이의 92%와 그 어머니의 97%에서 비타민 D 결핍(혈청 수치 25nmol/L 미만)이 확인된 반면, 비구루병 어린이에서는 22%, 아랍 어린이의 52%에서 확인되었습니다. 어머니( Dawodu 2005 ). 산모와 아이의 비타민 D 수치 사이에는 긍정적인 상관관계가 있는 것으로 나타났습니다.
또한, 전향적 종단적 연구인 Southampton Women's Survey에 참여한 임산부의 데이터를 사용한 분석에서는 비타민 D 상태가 낮은 산모의 태아에서 19주와 34주차에 대퇴골 골간단 단면적이 더 크고 대퇴골 벌어짐 지수가 더 높은 것으로 나타났습니다. ' 임신( Mahon 2010 ), 태아 대퇴골 부피와 비타민 D 상태 사이의 중요한 연관성( Ioannou 2012 ), 이는 초기 구루병 발생과 관련이 있을 수 있는 것으로 제안되었습니다( Harvey 2014 ).
비타민 D 상태와 면역 반응
비타민 D는 적응 면역 체계와 선천 면역 체계 모두에 직접적인 영향을 미칩니다( Miller 2010 ; Walker 2009 ). 어린이의 경우 비타민 D 부족은 제1형 당뇨병, 다발성 경화증, 알레르기 및 아토피성 질환과 같은 자가면역 질환과 관련이 있습니다( Bener 2009 ; Miller 2010 ; Pierrot‐Deseilligny 2010 ). 또한 다양한 연구에서는 비타민 D 결핍이 결핵, 폐렴 및 낭포성 섬유증과 밀접한 관련이 있으며( Chocano‐Bedoya 2009 ; Hall 2010 ; Nnoaham 2008 ; Williams 2008 ), 산전 및 주산기 비타민 D 결핍이 조기 호흡기에 영향을 미칠 수 있음을 보여주었습니다. 이 비타민은 폐 성장과 발달에 중요하므로 질병률이 높습니다( Devereux 2007 ; Litonjua 2009 ).
비타민 D는 대식세포와 내피 세포에 의한 항미생물 펩타이드 생산을 상향 조절함으로써( Wang 2004 ) 면역 체계에 긍정적인 영향을 미칠 수 있으며, 이는 바이러스를 비활성화하고 염증을 억제할 수 있으며( Cantorna 2008 ), 결과적으로 감염의 심각성을 줄일 수 있습니다.
비타민 D 독성
비타민 D 과잉은 신장 및 신장 결석과 관련된 고칼슘혈증(칼슘 수치가 10.5mg/dL 이상) 및 고칼슘뇨증(여성의 요로 칼슘 배설량이 250mg/dL을 초과)을 유발합니다( Heaney 2008 ). 성인의 독성은 일반적으로 10,000 IU(국제 단위)/일(250mcg/일)보다 높은 용량의 비타민 D에서 나타나지만, 대부분의 증거는 단기 노출(6개월 미만)을 기반으로 합니다( Hathcock 2007 ; Heaney 2008 ; IOM 2011 ; Vieth 1999 ). 7.5mg(300,000IU) 이상을 제공하는 단일 용량 보충제도 해로울 수 있습니다( Roth 2011a ).
쥐와 토끼를 대상으로 한 몇 가지 연구에서는 비타민 D로 인한 기형 발생(선천적 결손) 및 자손의 부작용(예: 성장 제한, 골화 지연, 두개안면 형성 저하)의 가능성이 제시되었습니다(Ariyuki 1987; Chan 1979 ; Friedman 1969 ; 오르노이 1968 , 오르노이 1969 ). 그러나 이러한 결과를 인간에게 추정하는 데는 상당한 한계가 있으며, 산모가 하루 5mg(200,000IU)의 비타민 D를 유지 용량으로 섭취한 후 태아에 대한 부작용이 발생하지 않은 것으로 보고되었습니다. 전반적으로, 동물 및 인간 연구에 따르면 산모의 농도가 정상 범위 내에 있을 때 태아의 비타민 D 대사산물 과잉이 발생할 가능성이 거의 없습니다( Roth 2011a ).
개입에 대한 설명
세계보건기구(WHO)는 현재 정기적인 산전 관리의 일환으로 임신 중 비타민 D 보충제 제공을 권장하지 않습니다( WHO 2016 ). 이는 주로 근거가 부족하고 미국 의회와 일치하는 VDD의 경우에만 해당되기 때문입니다. 산부인과 의사 및 산부인과 의사 지침( ACOG 2015 ).
전반적인 건강에 적합하거나 최적이라고 간주되는 25‐하이드록시비타민 D 수준에 관해 지속적인 논란이 있습니다. 미국 의학 연구소(US Institute of Medicine)는 현재 이용 가능한 연구( IOM 2011 ) 를 기반으로 50nmol/L 또는 20ng/mL보다 큰 농도가 적절하다고 결정했습니다 . 그러나 많은 연구자들은 최적 수준이 더 높아야 한다고 생각합니다(75nmol/L 이상). 또는 30ng/mL)( Dawson‐Hughes 2005 ; Hollick 2009 ). 25‐하이드록시비타민 D의 적절한 수준을 유지하기 위한 비타민 D 권장 사항도 조직마다 다릅니다. WHO/국제연합 식량농업기구가 정한 권장 영양소 섭취량(RNI)은 임산부의 비타민 D 200IU/일(5mcg/일)입니다( WHO 2004 ). 유럽식품안전청(EFSA)과 미국 의학연구소에서는 임산부에게 하루 600IU(15mcg)의 비타민 D를 권장합니다( EFSA 2016 ; IOM 2011 ). 왕립 산부인과 대학에서는 모든 임산부에게 하루 400IU(10mcg)를 권장합니다( RCOG 2014 ). 고위험 여성(검은색 피부, 햇빛 노출 감소, 사회적으로 소외되거나 비만인 여성)의 경우 최소 1000IU(25mcg/일)를 권장합니다. 또한 자간전증 위험이 높은 여성의 경우 칼슘과 함께 최소 800IU/일(20mcg/일)을 권장합니다. 중부 유럽의 전문가 패널은 하루 1500~2000IU(37.5~50.0mcg)를 권장했습니다( Pludowski 2013b ).
임신 중 비타민 D 보충제 사용에 대한 권장 사항도 200~400IU/일(5~10mcg/일) 범위로 다양합니다( Canadian Pediatric Society 2007 ; UK Department of Health 2009 ). 미국 소아과 학회( Wagner 2008 )는 산과 진료를 제공하는 의료 전문가가 임산부의 비타민 D 농도를 측정하여 산모의 비타민 D 상태를 모니터링하는 것을 고려해야 한다고 제안합니다. 여러 연구자들은 체내에서 비타민 D의 최적 수준을 달성하기 위해 1000~1600 IU(25~40 mcg/일)의 비타민 D 보충 용량이 필요할 수 있다고 제안했습니다( Dawson‐Hughes 2005 ). 이 용량은 25-하이드록시비타민 D 수치가 낮은 개인에게 경구 투여되는 비타민 D 3 1mcg(40IU)당 혈청 25-하이드록시비타민 D를 1.2nmol/L까지 증가시킬 것으로 예상됩니다 . 기준 농도가 더 높은 경우에는 동일한 용량에서 더 작은 증분을 갖게 됩니다( Dawson‐Hughes 2005 ). 다른 사람들은 임산부가 50nmol/L(20ng/mL) 이상의 혈중 비타민 D 농도를 유지하려면 약 1000IU/일의 복용량이 필요할 수 있다고 제안했습니다( Heaney 2003 ; Hollis 2004 ; Hollis 2007 ; Vieth 2001 ). 매주 5000IU(125mcg/주)( Utiger 1998 ) 또는 200,000IU(5mg) 이상의 단일 용량( Mallet 1986 ; Sahu 2009 ; Yu 2009 )과 같은 더 높은 용량도 제안되었습니다.
비타민 D는 햇빛에 노출되면 피부에서도 합성될 수 있으므로 최적의 혈청 수준에 도달하기 위해 일상적인 햇빛 노출을 늘리는 것이 권장됩니다( Holick 2002 ). 그러나 과도한 자외선은 발암물질이므로 식품이나 보충제를 통해 비타민 D를 추가로 섭취하는 것이 좋습니다.
개입이 어떻게 작동할 수 있는지
비타민 D 보충은 일부 연구에서 임신 중 산모의 비타민 D 상태를 개선하는 것으로 나타났으며( Delvin 1986 ; Yu 2009 ), 이는 결국 태아와 신생아의 비타민 D 공급에 직접적인 영향을 미칠 수 있습니다( Brooke 1980 ). 비타민 D 보충 의 추가적인 이점에 대한 정보는 제한적이지만 조산(임신 37주 미만) 및 저체중 출생(2,500g 미만)을 예방하는 데 있어 임신 중 비타민 D 보충의 잠재적 효과가 제안되었습니다( Maxwell 1981 ). 저체중 출생 위험에 대한 철분 및 엽산 보충과 같은 임신 중 다른 영양 중재보다 더 중요합니다( Christian 2003 ). 산모의 비타민 D 보충이 신생아 성장에 잠재적인 영향을 미칠 수도 있습니다( Marya 1988 ). 수유 중 모유 내 비타민 D의 적절한 농도를 보장하려면 임신 중 비타민 D 보충이 필요할 수 있습니다( Butte 2002 ). 그러나 임신 초기 비타민 D 상태가 산모 및 신생아 건강 결과의 중요한 결정 요인임을 시사하는 증거가 있으므로 임신 초기에 보충을 시작하면 이점을 볼 수 있다는 점에 유의하는 것이 중요합니다( Karras 2018 ).
이 검토를 수행하는 것이 중요한 이유
현재 대부분의 국가에서는 일상적인 산전 관리의 일부로 비타민 D 보충을 포함하지 않습니다. 뉴욕 과학 아카데미의 새클러 영양 과학 연구소와 빌 & 멜린다 게이츠 재단이 소집한 실무 그룹에서 언급한 바와 같습니다(비타민 D 결핍의 글로벌 유병률과 질병 부담을 평가하기 위해 과학 조직 위원회와 협력) ), 비타민 D는 임신과 출산 결과에 영향을 미치지만 증거는 상충됩니다( Roth 2018 ).
이 리뷰는 임신 중 비타민 D 보충에 관한 이전 Cochrane 리뷰를 업데이트합니다( De‐Regil 2016 ). 2016년 검토에는 15건의 임상시험(여성 2,833명)이 포함되었으며 임산부에게 비타민 D를 보충하면 자간전증, 저체중아 출산 및 조산의 위험을 줄일 수 있다고 결론지었습니다. 그러나 비타민D와 칼슘을 함께 섭취하면 조산 위험이 높아질 수 있습니다. 본 검토에는 산모와 신생아의 웰빙을 위한 임신 중 비타민 D 보충제의 효과와 안전성을 테스트한 임상시험의 새로운 증거가 포함되어 있습니다. 이 검토의 결과는 인구 수준에서 실무 지침을 확립하는 데 기여할 수 있습니다.
가장 효과적이고 안전한 복용량, 최적의 복용량 요법(매일, 간헐적 또는 단일 복용량), 비타민 D 보충 시작 시기, 다른 비타민 및 미네랄과 결합된 비타민 D의 효과에 대한 정보도 정책을 알리는 데 필요합니다. -만들기. 실제로 우리는 비타민 D 복용량과 그것이 임신 및 유아 결과에 미치는 영향을 비교하는 또 다른 체계적인 검토를 수행하고 있습니다( Palacios 2018 ).
목표
임신 중 여성에게 비타민 D 보충제를 단독으로 투여하거나 칼슘이나 다른 비타민 및 미네랄과 함께 투여하면 산모와 신생아의 결과를 안전하게 개선할 수 있는지 여부를 조사합니다.
행동 양식
이 검토를 위한 연구를 고려하는 기준
연구 유형
우리는 개인 또는 클러스터 수준에서 무작위 배정이 가능한 무작위 및 준 무작위 시험을 포함하려고 했으나, 개별 무작위 배정이 있는 무작위 대조 시험만 찾았습니다. 이 메타 분석에는 교차 시험이나 기타 관찰 설계(예: 코호트 또는 사례 대조 연구)를 포함하지 않았지만 관련이 있는 경우 토론에서 그러한 증거를 고려했습니다. 데이터를 추출하기에 충분한 정보가 있는 경우 초록을 포함했습니다.
참가자 유형
모든 국가에 거주하는 재태 연령, 출생연령, 출산력(출생 수) 및 태아 수에 관계없이 임신한 여성. 기존 질환이 있는 임산부는 제외되었습니다.
개입 유형
복용량, 기간, 보충 시작 시간, 보충 유형(경구 또는 주사)에 관계없이 임신 중 비타민 D 보충. 중재군과 대조군이 유사하게 치료되는 한 비타민 D를 단독으로 테스트하거나 다른 미량 영양소와 함께 테스트하는 임상시험을 포함했습니다. 구체적으로 우리는 다음과 같은 비교를 평가했습니다.
-
비타민 D 단독 보충 대 위약 또는 개입 없음(비타민이나 미네랄 없음)
-
비타민 D + 칼슘 보충 대 위약 또는 개입 없음(비타민 또는 미네랄 없음)
-
비타민 D + 칼슘 + 기타 비타민 및 미네랄 보충 대 칼슘 + 기타 비타민 및 미네랄 보충(비타민 D 없음)
-
비타민 D + 칼슘 보충 대 칼슘 보충(그러나 비타민 D는 없음)
-
비타민 D + 칼슘 + 기타 비타민 및 미네랄 보충 대 기타 비타민 및 미네랄 보충(비타민 D + 칼슘 없음)
결과 측정 유형
산모의 산전 임상 및 실험실 결과와 유아 임상 및 실험실 결과는 아래에 설명되어 있습니다.
주요 결과
산모
-
자간전증(시험 참가자가 정의한 대로).
-
임신성 당뇨병(시험자가 정의한 대로).
-
부작용(예: 고칼슘혈증, 신장 결석).
유아
-
조산(임신 기간 37주 미만).
-
저체중 출생(2500g 미만).
2차 결과
산모
-
내당능 장애(시험 참가자가 정의한 대로).
-
제왕 절개.
-
임신성 고혈압(시험자가 정의한 대로).
-
산모 사망(임신 중 또는 임신 종료 후 42일 이내 사망).
-
만기 비타민 D 농도(nmol/L 단위로 25‐하이드록시비타민 D).
유아
-
출생 길이(cm).
-
출생 시 머리둘레(cm).
-
출생 체중(g).
-
신생아기(분만 후 28일 이내) 동안 특별 진료(중환자실 포함)에 입원합니다.
-
사산(시험 참가자가 정의한 대로).
-
신생아 사망(분만 후 28일 이내)
-
Apgar 점수는 5분에 7 미만입니다.
-
신생아 감염(예: 출산 후 28일 이내에 호흡기 감염).
-
극조산(임신 기간 32주 미만).
연구 식별을 위한 검색 방법
본 리뷰의 다음 검색 방법 섹션은 Cochrane Pregnancy and Childbirth에서 사용하는 표준 템플릿을 기반으로 합니다.
전자 검색
이번 업데이트를 위해 정보 전문가에게 연락하여 Cochrane Pregnancy and Childbirth's Trials Register를 검색했습니다(2018년 7월 12일).
The Register는 임신 및 출산 분야에서 25,000개 이상의 대조 임상시험 보고서가 포함된 데이터베이스입니다. 이는 30년 이상의 검색 기간을 나타냅니다. CENTRAL, MEDLINE, Embase 및 CINAHL에 대한 세부 검색 전략을 포함하여 임신 및 출산 시험 등록을 채우는 데 사용되는 전체 최신 검색 방법 수기 검색된 저널 및 학회 논문집 목록, 현재 인식 서비스를 통해 검토된 저널 목록은 이 링크를 따라가세요.
간단히 말하면, Cochrane Pregnancy and Childbirth's Trials Register는 정보 전문가가 관리하며 다음에서 식별된 임상시험을 포함합니다.
-
Cochrane Central Register of Controlled Trials(CENTRAL)의 월별 검색;
-
MEDLINE(Ovid)의 주간 검색;
-
Embase(Ovid)의 주간 검색;
-
CINAHL(EBSCO)의 월별 검색;
-
30개의 저널과 주요 학회의 진행 과정을 수기 검색합니다.
-
추가 44개 저널에 대한 주간 최신 인식 알림과 월간 BioMed Central 이메일 알림.
검색 결과는 두 사람이 심사하며, 위에서 설명한 검색 활동을 통해 확인된 모든 관련 임상시험 보고서의 전문을 검토합니다. 설명된 중재에 따라 각 시험 보고서에는 특정 임신 및 출산 검토 주제(또는 주제)에 해당하는 번호가 할당된 다음 등록부에 추가됩니다. 정보 전문가는 키워드가 아닌 이 주제 번호를 사용하여 각 리뷰에 대한 등록을 검색합니다. 이로 인해 관련 검토 섹션( 포함된 연구 , 제외된 연구 , 분류 대기 중인 연구 , 진행 중인 연구 )에서 완전히 설명된 보다 구체적인 검색 세트가 생성됩니다.
또한 진행 중이거나 계획된 임상시험에 대해 ClinicalTrials.gov 및 WHO가 주최하는 국제 임상시험 등록 플랫폼(ICTRP)에서 레지스트리를 검색했습니다(2018년 7월 12일)( 부록 1 참조 ).
다른 리소스 검색
진행 중이거나 출판되지 않은 연구를 확인하기 위해 우리는 WHO 생식보건부, 건강 및 개발을 위한 연구 및 영양부, WHO 지역 사무소, 유엔 아동 기금(UNICEF), 국제 영양부(NI), 영양 개선을 위한 글로벌 연합(GAIN) 및 미국 질병 통제 예방 센터(CDC)(2018년 5월 15일)
날짜나 언어 제한을 적용하지 않았습니다.
데이터 수집 및 분석
이 검토의 이전 버전에서 사용된 방법은 De‐Regil 2016을 참조하세요 .
이번 업데이트에서는 업데이트된 검색 결과로 식별된 보고서를 평가하기 위해 다음 방법을 사용했습니다.
본 검토의 다음 방법 섹션은 Cochrane Pregnancy and Childbirth에서 사용하는 표준 템플릿을 기반으로 합니다.
연구 선택
두 명의 검토 저자(LK, CP)는 검색을 통해 식별된 모든 참고문헌의 포함 여부를 독립적으로 평가했습니다. 모든 논문은 2회에 걸쳐 평가되었으며, 의견 차이가 있을 경우 토론을 통해 해결하거나, 필요한 경우 세 번째 검토 저자(JP)와 상담했습니다.
연구가 초록으로만 출판되었거나 연구 보고서에 방법에 대한 정보가 거의 포함되어 있지 않은 경우, 우리는 연구 설계 및 결과에 대한 추가 세부 정보를 얻기 위해 저자에게 연락을 시도했습니다. 우리는 잠재적으로 적격한 모든 연구를 선별할 수 있었습니다.
데이터 추출 및 관리
우리는 데이터를 추출하는 양식을 디자인했습니다. 포함된 연구의 경우 모든 검토 저자는 합의된 형식을 사용하여 데이터를 추출했습니다. CP는 Review Manager 소프트웨어( RevMan 2014 )에 데이터를 입력했고 JP와 LK는 정확성을 확인했습니다.
평균 위험비 측면에서 이분형 데이터를 분석하고, 평균 차이 측면에서 연속 데이터를 분석했습니다. 임상시험이 다양한 규모의 결과를 보고하지 않았기 때문에 표준 평균 차이를 사용할 필요가 없었습니다.
포함된 연구의 비뚤림 위험 평가
두 명의 검토 저자(CP, LK)는 Cochrane Handbook for Systematic Reviews of Interventions ( Higgins 2011 ) 에 설명된 기준을 사용하여 각 연구의 비뚤림 위험을 독립적으로 평가했습니다 . 의견 차이가 있는 경우 토론을 통해 해결하고 제3저자(JP)와 상의했습니다.
(1) 무작위 시퀀스 생성(선택 편향 가능성 확인)
우리는 포함된 각 연구에 대해 비교 가능한 그룹을 생성해야 하는지 여부를 평가할 수 있을 만큼 충분히 자세하게 할당 순서를 생성하는 데 사용된 방법을 설명했습니다.
우리는 방법을 다음과 같이 평가했습니다.
-
편향 위험이 낮음(완전한 임의 프로세스, 예: 난수 테이블, 컴퓨터 난수 생성기)
-
편향 위험이 높음(무작위가 아닌 프로세스, 예: 홀수 또는 짝수 생년월일, 병원 또는 진료소 기록 번호)
-
편견의 위험이 불분명합니다.
(2) 할당 은폐(선택 편향 가능성 확인)
우리는 포함된 각 연구에 대해 할당 순서를 숨기는 데 사용된 방법을 설명하고 중재 할당이 모집 전이나 도중에 예측될 수 있었는지 또는 할당 후 변경될 수 있었는지 평가했습니다.
우리는 다음과 같이 방법을 평가했습니다.
-
낮은 편향 위험(예: 전화 또는 중앙 무작위 배정, 연속 번호가 매겨진 봉인된 불투명 봉투)
-
편향 위험이 높음(개방형 무작위 할당, 봉인되지 않거나 불투명하지 않은 봉투)
-
불분명하다.
(3.1) 참가자 및 직원의 눈가림(가능한 성과 편향 확인)
우리는 포함된 각 연구에 대해 참가자가 어떤 개입을 받았는지에 대한 지식을 연구 참가자와 직원에게 맹검하는 데 사용된 방법을 설명했습니다. 눈가림이 되어 있거나 눈가림이 부족하여 결과에 영향을 미칠 가능성이 없다고 판단한 경우 연구가 비뚤림 위험이 낮다고 생각했습니다. 다양한 결과 또는 결과 클래스에 대해 별도로 눈가림을 평가했습니다.
우리는 다음과 같이 방법을 평가했습니다.
-
참가자에 대한 편견의 위험이 낮거나 높거나 불분명합니다.
-
직원에 대한 편향 위험이 낮거나 높거나 불분명합니다.
임상시험의 맹검 상태가 불분명하거나 임상시험이 공개된 경우 맹검을 '비뚤림 위험이 높음'으로 분류했습니다.
(3.2) 결과 평가의 눈가림(가능한 탐지 편향 확인)
우리는 포함된 각 연구에 대해 참가자가 어떤 개입을 받았는지에 대한 지식을 결과 평가자가 보지 못하게 하기 위해 사용된 방법을 설명했습니다. 다양한 결과 또는 결과 클래스에 대해 별도로 눈가림을 평가했습니다.
우리는 결과 평가를 맹검하는 데 사용된 방법을 다음과 같이 평가했습니다.
-
편향 위험이 낮음;
-
편견의 위험이 높습니다.
-
불분명하다.
(4) 불완전한 결과 데이터(탈락, 탈락, 프로토콜 이탈 등을 통한 이탈 편향 가능성 확인)
우리는 각 시험에 대해 체계적으로 후속 조치 및 무작위 배정 후 제외에 대한 손실을 평가했습니다.
우리는 포함된 각 연구와 각 결과 또는 결과 클래스에 대해 분석에서 감소 및 제외를 포함한 데이터의 완전성을 설명했습니다. 감소 및 제외가 보고되었는지 여부, 각 단계에서 분석에 포함된 숫자(전체 무작위 참가자와 비교), 보고된 경우 감소 또는 제외 이유, 누락된 데이터가 그룹 간에 균형을 이루거나 결과와 관련되었는지 여부를 기록했습니다. 우리는 다음과 같이 방법을 평가했습니다.
-
편향 위험이 낮음;
-
편견의 위험이 높습니다.
-
불분명하다.
처음에 무작위로 배정된 참가자의 80% 이상이 분석에 포함되었고 모든 손실이 그룹 간에 균형을 이루었다면 후속 조치를 '비뚤림 위험이 낮음'으로 간주했습니다. 처음에 무작위로 배정된 참가자의 비율이 분석에 포함되었는지는 확실하지 않습니다. 불분명하며, 처음에 무작위로 배정된 환자의 80% 미만이 분석에 포함되었거나 손실이 여러 치료 그룹에서 불균형한 경우 '비뚤림 위험이 높습니다'.
(5) 선택적 보고(보고편향 확인)
우리는 포함된 각 연구에 대해 선택적 결과 보고 편향 가능성을 조사한 방법과 발견한 내용을 설명했습니다.
우리는 다음과 같이 방법을 평가했습니다.
-
낮은 비뚤림 위험(연구의 사전 지정된 모든 결과와 검토에 관심이 있는 모든 예상 결과가 보고된 것이 분명한 경우)
-
비뚤림 위험이 높음(연구의 사전 지정된 결과가 모두 보고되지 않은 경우, 보고된 하나 이상의 기본 결과가 사전 지정되지 않은 경우, 관심 있는 결과가 불완전하게 보고되어 사용할 수 없음, 연구에 주요 결과가 포함되지 않은 경우) 보고되었을 것으로 예상되는 결과)
-
편견의 위험이 불분명합니다.
(6) 기타 편견의 원인
우리는 각 연구에 비뚤림 위험을 초래할 수 있는 다른 문제가 없는지 평가했습니다. 포함된 각 연구에 대해 다른 가능한 비뚤림 원인에 대해 가지고 있는 중요한 우려 사항을 언급했습니다.
-
추가 편견의 위험이 낮습니다.
-
추가 편견의 위험이 높습니다.
-
추가 편향의 위험이 있는지 여부는 불분명합니다.
(7) 전반적인 편향 위험
우리는 연구 내(영역 간)와 연구 간 두 가지 수준에서 편향 위험을 요약했습니다.
첫 번째로, 우리는 Cochrane Handbook for Systematic Reviews of Interventions ( Higgins 2011 )에 제공된 기준에 따라 연구가 비뚤림 위험이 높은지 여부에 대해 명시적으로 판단했으며, 주요 결과에 대해 편견 수준의 영향을 조사했습니다. 민감도 분석을 수행함으로써 .
GRADE 접근법을 사용한 근거의 확실성 평가
연구 전반에 걸친 평가를 위해 검토의 주요 결과는1 번 테이블;표 2그리고표 3, GRADE 프로파일러(GRADEpro) 지침 개발 도구( GRADEpro 2015 )를 사용하여 작성되었습니다. 각 비교에 대한 주요 결과는 가능한 경우 해당 결과에 데이터를 제공하는 참가자 및 연구 수와 함께 상대 효과 추정치와 함께 나열됩니다. 각 결과에 대해 두 명의 검토 저자가 Grading of Recommendations Assessment, Development and Evaluation(GRADE) 핸드북( GRADE 핸드북 ) 을 사용하여 연구 내 비뚤림 위험(방법론적 품질), 직접성 등을 고려하여 근거의 확실성을 독립적으로 평가 했습니다. 증거, 이질성, 효과 추정의 정확성 및 출판 편향 위험; 이는 네 가지 수준의 확실성(높음, 보통, 낮음 또는 매우 낮음) 중 하나를 의미합니다. 이 평가는 이 검토에 포함된 임상시험으로만 제한되었습니다.
치료 효과 측정
이분법적 데이터
이분형 데이터의 경우 결과를 95% 신뢰 구간의 평균 위험 비율로 표시합니다.
지속적인 데이터
연속 데이터의 경우 결과가 시험 간에 동일한 방식으로 측정되었으므로 평균 차이를 사용했습니다. 시험을 결합하기 위해 표준화된 평균 차이를 사용할 필요가 없었습니다.
분석 단위 문제
군집 무작위 시험
개별 무작위 임상시험과 함께 분석에 군집 무작위 임상시험을 포함할 계획이었지만 이 설계에 적합한 연구를 찾지 못했습니다. 이를 허용할 만큼 충분한 정보가 있는 경우, 중재의 체계적 검토를 위한 Cochrane Handbook ( Higgins 2011 ) 에 설명된 방법을 사용하여 군집 무작위 연구 결과의 표준 오차를 조정할 계획이었습니다 . 우리는 시험(가능한 경우)이나 다른 소스에서 파생된 클러스터 내 상관 계수(ICC)의 추정치를 사용할 계획이었습니다. 다른 소스의 ICC가 사용된 경우 이를 보고하고 민감도 분석을 수행하여 ICC의 변동 효과를 조사할 계획이었습니다.
클러스터 무작위 임상시험과 개별 무작위 임상시험을 모두 식별했다면, 연구 설계 사이에 이질성이 거의 없고 중재 효과와 무작위 배정 단위 선택 사이의 상호 작용이 다음과 같이 간주된다면 두 결과를 결합했을 것입니다. 할 것 같지 않은.
2개 이상의 치료군을 대상으로 한 연구
2개 이상의 개입 그룹이 포함된 연구(다군 연구)의 경우 그룹을 결합하여 단일 쌍별 비교를 생성하고( Higgins 2011 ) 해당 하위 그룹 범주에 세분화된 데이터를 포함했습니다. 두 개 이상의 연구 부문에서 대조군을 공유하는 경우, 참가자를 이중으로 계산하는 것을 방지하기 위해 대조군(사건 및 전체 인구)을 관련 하위 그룹 범주 수로 나누었습니다. 자세한 내용은 포함된 연구의 특성 표에 설명되어 있습니다.
교차 시험
우리는 포함할 수 있는 교차 시험을 고려하지 않았습니다.
누락된 데이터 처리
포함된 연구에 대해 우리는 감소 수준을 기록했습니다. 민감도 분석을 사용하여 치료 효과의 전반적인 평가에 누락된 데이터 수준이 높은 연구를 포함하는 경우의 영향을 조사했습니다.
모든 결과에 대해 가능한 한 치료 의도를 기준으로 분석을 수행했습니다. 즉, 각 그룹에 무작위로 배정된 모든 참가자를 분석에 포함시키고 할당된 그룹의 모든 참가자를 분석했습니다. , 할당된 개입을 받았는지 여부에 관계없이. 각 시험의 각 결과에 대한 분모는 무작위로 추출된 숫자에서 결과가 누락된 것으로 알려진 참가자를 뺀 숫자입니다.
이질성 평가
Tau², I² 및 Chi² 통계를 사용하여 각 메타 분석에서 통계적 이질성을 평가했습니다. 우리는 I²가 30%보다 크고 Tau²가 0보다 크거나 이질성에 대한 Chi² 테스트에서 낮은 P 값(0.10 미만)이 있는 경우 이질성을 실질적인 것으로 간주했습니다.
보고 편향 평가
우리는 10개 이상의 연구에서 주요 결과에 대한 깔때기 도표를 사용하여 보고 편향(예: 출판 편향)을 조사했습니다. 깔때기 플롯 비대칭성을 시각적으로 평가했습니다.
데이터 합성
Review Manager 소프트웨어( RevMan 2014 ) 를 사용하여 통계 분석을 수행했습니다 . 우리는 연구가 동일한 기본 치료 효과를 추정하고 있다고 가정하는 것이 합리적인 경우 데이터를 결합하기 위해 고정 효과 메타 분석을 사용하려고 했습니다. 즉, 임상시험이 동일한 개입을 조사하고 임상시험의 모집단과 방법이 충분히 유사하다고 판단된 경우 .
상당한 이질성을 발견했기 때문에 무작위 효과 메타 분석을 사용하여 임상시험 전반에 걸쳐 평균 치료 효과에 대한 전반적인 요약을 작성했습니다. 우리는 무작위 효과 요약을 가능한 치료 효과의 평균 범위로 취급했으며, 시험마다 다른 치료 효과의 임상적 의미를 논의했습니다. 평균 치료 효과가 임상적으로 의미가 없는 경우에는 임상시험을 통합하지 않았습니다.
무작위 효과 분석을 사용하여 결과를 95% 신뢰 구간과 Tau² 및 I² 추정치를 사용하여 평균 치료 효과로 제시합니다.
하위 그룹 분석 및 이질성 조사
우리는 다음과 같이 하위 그룹 분석을 사용하여 주요 결과에 대한 실질적인 이질성을 조사할 계획이었습니다.
-
보충 시작 시: 임신 20주 미만 대 임신 20주 이상 대 알 수 없음/혼합;
-
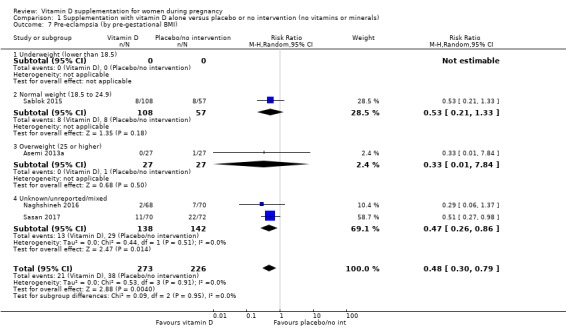
임신 전 체질량 지수(BMI)(kg/m 2 ) 기준: 저체중(18.5 미만) 대 정상 체중(18.5~24.9) 대 과체중(25 이상) 대 알 수 없음/혼합
-
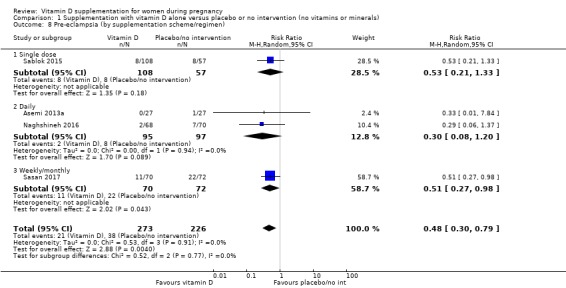
보충 계획/요법별: 단일 대 매일 대 매주 대 알 수 없음/혼합;
-
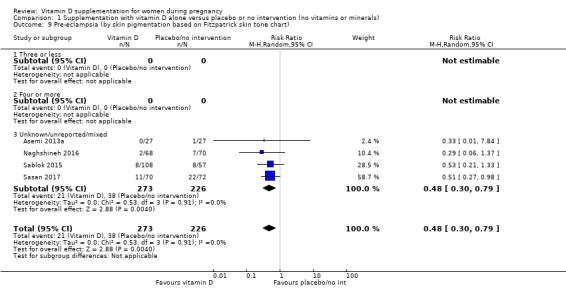
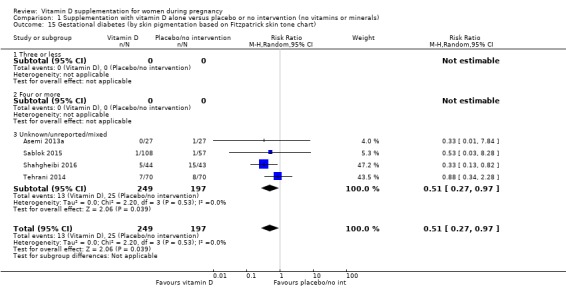
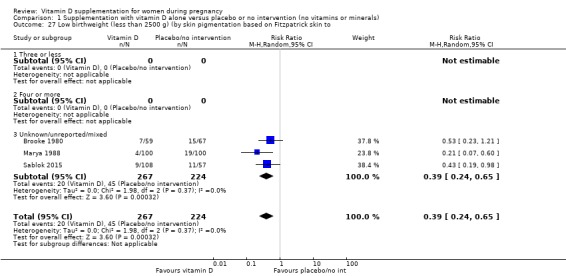
Fitzpatrick 피부톤 차트를 기반으로 한 피부 색소 침착( Fitzpatrick 1988 ): 3개 이하 대 4개 이상 대 혼합/알 수 없음;
-
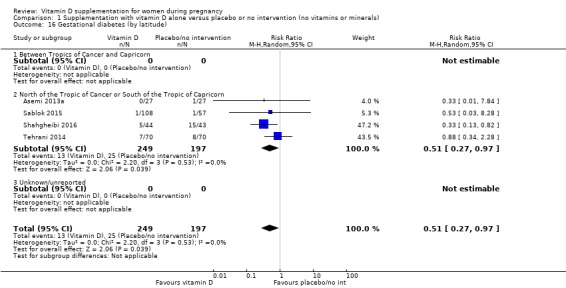
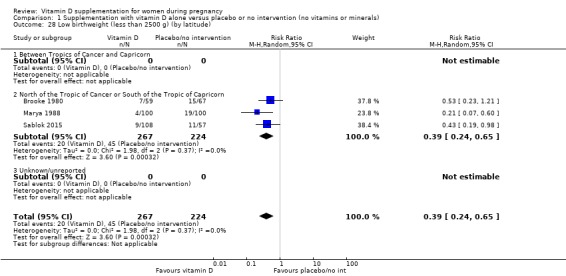
위도 기준: 북회귀선과 남회귀선 사이 대 북회귀선 또는 남회귀선 대 알 수 없음/혼합;
-
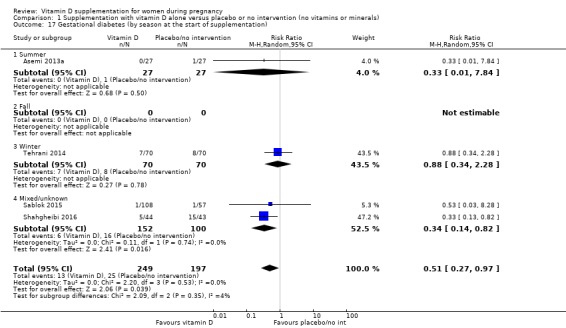
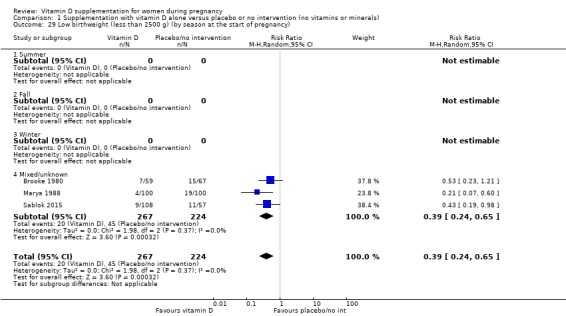
임신 시작 시 계절별: 여름 대 겨울 대 혼합/알 수 없음/보고되지 않음.
실질적으로 우리는 3회 이하의 임상시험을 통해 해당 결과에 대해 하위그룹 분석을 수행하지 않기로 결정했습니다.
RevMan( RevMan 2014 ) 내에서 사용할 수 있는 상호 작용 테스트를 통해 하위 그룹 차이를 평가했습니다 . Chi² 통계와 P 값, 상호 작용 테스트 I² 값을 인용한 하위 그룹 분석 결과를 보고했습니다.
민감도 분석
연구의 질을 바탕으로 민감도 분석을 실시하려고 했으나, 단 하나의 연구만이 높은 질로 간주되었기 때문에 이 분석을 수행하지 않았습니다. 무작위화와 할당 은폐 모두에서 비뚤림 위험이 낮고, 눈가림이나 추적 관찰 손실에서 비뚤림 위험이 낮은 것으로 평가된 경우 연구의 질이 높은 것으로 간주했습니다. 향후 업데이트에서는 무작위화 단위(해당하는 경우)의 효과를 조사하기 위해 민감도 분석을 수행할 것입니다.
결과
연구 설명
검색 결과
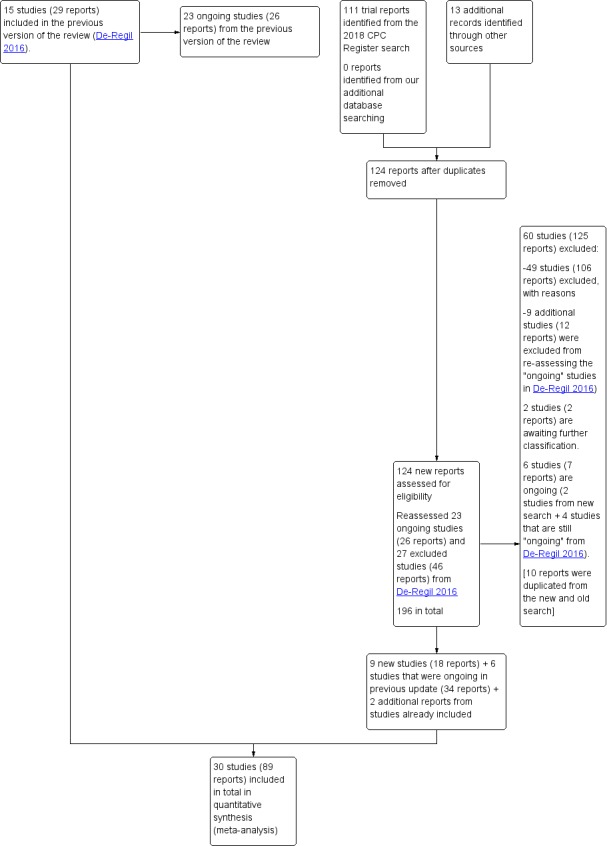
Cochrane Pregnancy and Childbirth's Trials Register 검색에서 총 111개의 새로운 보고서(중복 항목 제거 후), 추가 검색에서 13개의 보고서를 받았으며, 진행 중인 23개의 임상시험(26개 보고서)과 27개의 제외된 임상시험(46개 보고서)도 재평가했습니다. 이전 버전의 리뷰( De‐Regil 2016 )에서 따왔습니다. 보다:그림 1.
이번 업데이트에는 총 30개의 시험이 포함되었습니다. 이전 업데이트에는 15개가 이미 포함되었습니다( Asemi 2012 , Asemi 2013a , Brooke 1980 , Delvin 1986 , Diogenes 2013 , Grant 2013 , Li 2000a , Mallet 1986 , Marya 1987 , Marya 1988 , Mazurkevich 2013 , Roth 2010 , Sablo k 2015 , 타헤리안 2002 ; 유 2008 ). 업데이트된 검색을 통해 9개의 새로운 임상시험을 식별했으며( Kaur 1991 , Naghshineh 2016 , Sabet 2012 , Samimi 2016 , Samimi 2017 , Sasan 2017 , Shahgheibi 2016 , Singh 2015 , Vaziri 2016 ) 이전에 진행 중인 것으로 분류된 6개의 추가 임상시험을 포함했습니다. 업데이트( Benson 2009 ; Bhutta 2011 ; Harvey 2012 ; Mirghafourvand 2013 ; Roth 2013 ; Tehrani 2014 ).
우리는 발표된 다른 연구( Karamali 2015 )와 동일한 결과를 나타내는 여러 결과가 있었기 때문에 정보의 진실성에 대한 우려를 제기한 또 다른 연구( Qian 2015 )를 확인했습니다. 우리는 출판 윤리 위원회(COPE)의 지침에 따라 두 저널의 편집자들( Cope 2016 )과 함께 문제를 조사했으며 출판물( Qian 2015 )은 2018년 8월 20일에 편집자들에 의해 철회되었습니다. 따라서 이 재판은 옮겨졌습니다. 제외합니다.
총 60건의 임상시험(125개 보고서)을 제외했습니다. 진행 중이거나 출판되지 않은 임상시험 6건을 확인했습니다( Baird 2016 ; Jelsma 2013 ; Judkins 2010 ; Lindqvist 2010 ; Mosalanejad 2016 ; Rasmussen 2009 ). 데이터 추출을 위한 정보가 충분하지 않고 추상 형식으로만 제공되었기 때문에 분류를 기다리는 두 가지 임상시험이 있습니다( Bimson 2017 ; Das 2009 ).
이러한 임상시험에 대한 자세한 내용은 다음 항목에 나와 있습니다. 포함된 연구의 특성 ; 제외된 연구의 특성 ; 분류 테이블을 기다리는 연구입니다 .
포함된 연구
이 업데이트된 검토에는 30건의 임상시험(7033명의 여성과 영유아 포함)이 포함되었습니다( Asemi 2012 , Asemi 2013a , Benson 2009 , Bhutta 2011 , Brooke 1980 , Delvin 1986 , Diogenes 2013 , Grant 2013 , Harvey 2012 , Kaur 1991 , Li 200 ). 0a ; Mallet 1986 , Marya 1987 , Marya 1988 , Mazurkevich 2013 , Mirghafourvand 2013 , Naghshineh 2016 , Roth 2010 , Roth 2013, Sabet 2012 , Sablok 2015 , Samimi 2016 , Samimi 2017 , Sasan 2017 , 샤게이비 2016 , 싱 2015 , 타헤리안 2002 , 테흐 라니 2014 , Vaziri 2016 , Yu 2008 ). 이러한 시험에 대한 자세한 내용은 포함된 연구의 특성 표 에 나와 있습니다 .
설정
이 검토에 포함된 임상시험은 1980년대부터 2015년까지 수행되었습니다.
시험은 호주( Benson 2009 ), 방글라데시( Roth 2010 ; Roth 2013 ), 브라질( Diogenes 2013 ), 중국( Li 2000a ) , 프랑스( Delvin 1986 ; Mallet 1986 ), 인도( Kaur 1991 ; Marya 1987 ; Marya 1988) 에서 수행되었습니다. , Sablok 2015 , Singh 2015 ), 이란 ( Asemi 2012 , Asemi 2013a , Mirghafourvand 2013 , Naghshineh 2016 , Sabet 2012 , Samimi 2016 , Samimi 2017 , Sasan 2017 , Shahgheibi 2016 , Taherian 2002 ; Tehrani 2014 ; Vaziri 2016 ) , 뉴질랜드( Grant 2013 ), 파키스탄( Bhutta 2011 ), 러시아( Mazurkevich 2013 ) 및 영국( Brooke 1980 ; Harvey 2012 ; Yu 2008 ).
위도
대부분의 시험은 북회귀선과 염소자리 위나 아래에서 수행되었습니다( Asemi 2012 ; Asemi 2013a ; Brooke 1980 ; Delvin 1986 ; Kaur 1991 ; Li 2000a ; Mallet 1986 ; Marya 1987 ; Marya 1988 ; Mazurkevich 2013 ; Mirghafourvand 2013 , 나그샤인 2016 , Roth 2010 , Roth 2013 , Sablok 2015 , Taherian 2002 , Yu 2008 , Sabet 2012 , Samimi 2016 , Samimi 2017 , Sasan 2017 , Shahgheibi 2016 , Vaziri 2016 , Benson 2009 , Bhutta 2011 , 테흐라니 2014 , 하비 2012 ). 북회귀선과 염소자리 사이에는 단 두 번의 실험만 수행되었으며( Grant 2013 ; Singh 2015 ), 한 연구는 염소자리 거짓말에 대해서만 수행되었습니다( Diogenes 2013 ).
계절성
계절은 겨울-봄 기간 동안 발생하는 일부 실험과 함께 실험마다 다양했습니다( Delvin 1986 ). 겨울( Mallet 1986 ; Naghshineh 2016 ; Tehrani 2014 ); 여름( Roth 2010 ; Yu 2008 ); 봄-여름 기간( Asemi 2013a ), 가을( Samimi 2016 ; Vaziri 2016 ), 13개 임상시험( Asemi 2012 ; Benson 2009 ; Bhutta 2011 ; Kaur 1991 ; Li 2000a ; Marya 1987 ; Marya 1988 ; Mazurkevich 2013 )에서 알 수 없음/보고되지 않음 ; 사베트 2012년 , Sasan 2017 , Shahgheibi 2016 , Singh 2015 , Taherian 2002 ) 또는 혼합( Brooke 1980 , Diogenes 2013 , Grant 2013 , Harvey 2012 , Mirghafourvand 2013 , Roth 2013 , Sablok 2015 , Samimi 2) 017 ).
참가자들
모든 시험의 표본 크기는 여성 40명( Delvin 1986 )에서 여성 1,560명( Roth 2013 ) 사이였습니다.
임신 전 체질량 지수(kg/m 2 )
참가자의 임신 전 체질량 지수(BMI)는 5개의 시험에서만 보고되었습니다( Asemi 2012 ; Asemi 2013a ; Diogenes 2013 ; Sablok 2015 ; Taherian 2002 ). 나머지 임상시험에서는 이를 보고하지 않았습니다. 무작위 배정 전 개입 전 BMI(kg/m 2 단위 , 30 미만 및 30 이상) 에 대해 계층화된 한 연구 ( Asemi 2013a ).
Fitzpatrick 피부톤 차트를 기반으로 한 피부 색소 침착
Fitzpatrick 피부톤 차트를 사용한 실험은 없었습니다( Fitzpatrick 1988 ). 그러나 여러 임상시험에서는 참가자의 민족성/인종을 보고했습니다. 대부분의 재판은 중동 여성을 대상으로 이루어졌습니다( Asemi 2012 , Asemi 2013a , Brooke 1980 , Bhutta 2011 , Tehrani 2014 , Mirghafourvand 2013 , Naghshineh 2016 , Sabet 2012, Samimi 2016 , Samimi 2017 , Sasan 2017 , Shahgheibi ). 2016년 , 타헤리안 2002년 , 바지 리 2016 ) 또는 아시아( Kaur 1991 ; Li 2000a ; Marya 1987 ; Marya 1988 ; Roth 2010 ; Roth 2013 ; Sablok 2015 ; Singh 2015 ). 두 건의 임상시험에서는 참가자가 혼합 민족( Benson 2009 ; Yu 2008 ) 출신이고 , 두 건의 임상시험은 백인( Harvey 2012 ; Mallet 1986 ), 백인 여성 또는 흑인 여성( Diogenes 2013 ), 그리고 다른 하나는 태평양, 유럽 및 마오리인이라고 보고했습니다. 여성( Grant 2013 ). 두 번의 임상시험에서는 참가자의 인종이나 출신 특성을 보고하지 않았습니다( Delvin 1986 ; Mazurkevich 2013 ).
개입
총 22건의 임상시험에서 비타민 D 보충제 제공을 위약 또는 무개입과 비교했습니다(비교 1: Asemi 2013a ; Benson 2009 ; Bhutta 2011 ; Brooke 1980 ; Delvin 1986 ; Grant 2013 ; Harvey 2012 ; Kaur 1991 ; Mallet 1986 ; Marya 1988년 , Mirghafourvand 2013 , Naghshineh 2016 , Roth 2010 , Sabet 2012 , Sablok 2015 , Samimi 2017 , Sasan 2017 , Shahgheibi 2016 , Singh 2015 , Tehrani 2014 , Vaziri 2016 , Yu 200 8 ).
총 9건의 임상시험에서 경구 비타민 D와 칼슘 보충제의 제공과 중재 없음 또는 위약을 비교했습니다(비교 2: Asemi 2012 ; Asemi 2013a ; Diogenes 2013 ; Li 2000a ; Marya 1987 ; Mazurkevich 2013 ; Mirghafourvand 2013 ; Samimi 2016 ; Taherian 2002 ) . Mirghafourvand 2013 의 연구는 비타민 D 단독 및 비타민 D + 칼슘을 위약과 비교하여 두 비교에 모두 포함되었습니다.
경구용 비타민 D와 칼슘, 철, 엽산을 칼슘, 철, 엽산과 비교한 임상시험은 단 한 건뿐이었지만 비타민 D는 비교하지 않았습니다(비교 4: Roth 2013 ).
경구용 비타민 D + 칼슘 보충제 대 칼슘(비교 3), 경구용 비타민 D + 칼슘 + 기타 비타민 및 미네랄 보충제 대 기타 경구용 비타민 및 미네랄 보충제(비타민 D + 칼슘 없음)의 효과를 평가한 임상시험은 없습니다(비교 5 ).
보충 시작
총 7개의 임상시험이 20주차 이전에 보충을 시작했습니다( Benson 2009 ; Bhutta 2011 ; Harvey 2012 ; Naghshineh 2016 ; Samimi 2017 ; Singh 2015 ; Tehrani 2014 ). 나머지 시험에서는 임신 20주 이상에 보충을 시작했습니다( Asemi 2012 ; Asemi 2013a ; Brooke 1980 ; Delvin 1986 ; Diogenes 2013 ; Grant 2013 ; Kaur 1991 ; Li 2000a ; Mallet 1986 ; Marya 1987 ; Marya 1988 ; Mazurkevich 2013년 , Mirghafourvand 2013 , Roth 2010 , Roth 2013 , Sabet 2012 , Sablok 2015 , Samimi 2016 , Sasan 2017 , Shahgheibi 2016 , Taherian 2002 , Vaziri 2016 , Yu 2008 ).
사용된 비타민 D의 복용량
제공된 비타민 D의 용량은 포함된 임상시험과 요법에 따라 다양했습니다.
시험은 보충 빈도가 달랐으며 일부 시험에서는 일일 복용량, 주간 복용량, 월간 복용량 또는 단일 복용량을 사용했습니다. 일부 임상시험에는 두 개 이상의 비타민 D 개입 그룹이 포함되었습니다.
일일, 주간 및 월간 복용량의 경우 하루 총량을 국제 단위(IU)로 계산했습니다. 사용된 일일 복용량은 5번의 시험에서 200IU 비타민 D였습니다( Asemi 2012 ; Diogenes 2013 ; Li 2000a ; Mazurkevich 2013 ; Taherian 2002 ). 세 번의 시험에서 400 IU 비타민 D( Asemi 2013a ; Li 2000a ; Samimi 2017 ); 두 번의 시험에서 600 IU 비타민 D( Naghshineh 2016 ; Roth 2013 ); 또 다른 시험에서는 800 IU 비타민 D( Yu 2008 ); 6번의 시험에서 1000 IU 비타민 D( Brooke 1980 ; Delvin 1986 ; Grant 2013 ; Harvey 2012 ; Mirghafourvand 2013 ; Mallet 1986 ); 두 번의 실험에서 1200 IU 비타민 D( Kaur 1991 ; Marya 1987 ); 세 번의 시험에서 2000 IU 비타민 D( Grant 2013 ; Singh 2015 ; Vaziri 2016 ); 한 번의 시험에서 2400 IU 비타민 D( Roth 2013 ); 5건의 시험에서 3333~3500IU의 비타민 D( Sabet 2012 ; Samimi 2016 ; Sasan 2017 ; Tehrani 2014 ); 두 번의 실험에서 4000 IU 비타민 D( Bhutta 2011 ; Roth 2013 ), 한 번의 실험에서 5000 IU 비타민 D( Shahgheibi 2016 ). 한 연구에서는 하루 2000IU로 보충을 시작했고, 임신 28주까지 25(ODH)‐D 수준이 75nmol/L 미만인 경우 복용량을 하루 4000IU로 두 배 늘렸습니다( Benson 2009 ). 한 연구에서는 또한 두 그룹 모두에게 하루 400mg의 질 프로게스테론이 함유된 젤을 제공했습니다( Samimi 2017 ). Roth 2013 의 연구에서는 위에서 언급한 것처럼 임신 중에 세 가지 다른 복용량을 제공했습니다. 주당 4200IU 또는 하루 600IU; 주당 16,800IU 또는 하루 2400IU; 주당 28,000IU 또는 하루 4000IU. 우리는 이 그룹의 데이터를 결합했으며 평균적으로 이 그룹은 주당 16,333IU 또는 하루 2333IU를 받았습니다.
비타민 D의 단일 용량 보충의 경우 용량은 한 연구에서 그룹당 200,000 IU 비타민 D까지 다양했습니다( Yu 2008 ). 한 번의 시험에서 600,000 IU 비타민 D( Marya 1988 ); 그리고 60,000 IU 비타민 D를 2회 투여합니다( Kaur 1991 ). 매달 100,000개의 비타민 D를 사용한 임상시험도 있었습니다( Sabet 2012 ). 2주마다 50,000회 복용량을 사용한 세 가지 시험( Tehrani 2014 ; Samimi 2016 ; Sasan 2017 ); 매주 35,000 IU의 비타민 D를 사용한 한 번의 시험( Roth 2010 ). Sablok 2015 연구에서 용량은 기준선의 혈청 25(OH)‐D 수준에 따라 달라졌습니다. 60,000 IU(혈청 25(OH)‐D 수준이 > 50 nmol/L인 경우) 1회 용량, 120,000 IU(혈청 25(OH)-D 수준이 25~50 nmol/L인 경우) 2회 용량으로 다양했습니다. 또는 120,000 IU의 4회 용량(혈청 25(OH)‐D 수준이 < 25 nmol/L인 경우).
전반적으로, 임신 기간 동안 제공되는 보충 비타민 D의 총 공급량은 다양했습니다. 16개의 시험에서는 56,000 IU 이하의 비타민 D가 제공되었습니다( Asemi 2012 ; Asemi 2013a ; Benson 2009 ; Delvin 1986 ; Diogenes 2013 ; Grant 2013 ; Harvey 2012 Li 2000a ; Mazurkevich 2013 ; Naghshineh 2016 ; Roth 2013 ; Sabet 2012년, 사미미 2017년 , 싱 2015 년 , Taherian 2002 , Vaziri 2016 ); 9건의 시험에서는 56,000~200,000IU 이상의 비타민 D를 제공했습니다( Bhutta 2011 ; Brooke 1980 ; Kaur 1991 ; Mallet 1986 ; Marya 1987 ; Mirghafourvand 2013 ; Roth 2013 ; Sablok 2015 ; Yu 2008 ). 7건의 임상시험에서는 임신 기간 동안 200,000IU 이상의 비타민 D를 제공했습니다( Marya 1988 ; Roth 2010 ; Roth 2013 ; Sablok 2015 ; Samimi 2016 ; Sasan 2017 ; Tehrani 2014 ). 한 연구에서는 보충이 언제 시작되었는지 명시하지 않았기 때문에 이를 추정할 수 없었습니다( Shahgheibi 2016 ).
사용되는 비타민 D 형태
비타민 D는 20건의 시험에서 콜레칼시페롤‐D3의 형태로 제공되었습니다( Asemi 2012 ; Asemi 2013a ; Benson 2009 ; Delvin 1986 ; Diogenes 2013 ; Grant 2013 ; Harvey 2012 ; Kaur 1991 ; Li 2000a ; Mazurkevich 2013 ; Roth 2010 ; 로스 2013년 , Sabet 2012년 , Sablok 2015년, Samimi 2016 년 , Samimi 2017년 , Sasan 2017 년 , Singh 2015년 , Taherian 2002년 , Vaziri 2016년 ) 세 번의 시험에서 ergocalciferol‐D2로 사용되었습니다( Brooke 1980 , Mallet 1986 , Yu 2008 ). . 7건의 임상시험에서는 사용된 비타민 D 형태를 보고하지 않았습니다( Bhutta 2011 ; Marya 1987 ; Marya 1988 ; Mirghafourvand 2013 ; Naghshineh 2016 ; Shahgheibi 2016 ; Tehrani 2014 ).
비타민 D와 칼슘 보충을 제공하는 실험에서 칼슘의 복용량
비타민 D와 함께 제공되는 칼슘의 복용량은 300mg( Mirghafourvand 2013 ), 375mg( Marya 1987 ); 500mg( Asemi 2012 ; Asemi 2013a ; Roth 2013 ; Taherian 2002 ); 칼슘 600mg( Diogenes 2013 ; Li 2000a ), 1000mg( Samimi 2016 ) 및 1250mg( Mazurkevich 2013) . 모두 탄산칼슘을 사용했습니다.
보건 종사자 간부
임상시험은 대부분 산전 관리와 보충제 투여라는 맥락에서 수행되었으며, 산전 관리는 연구자 자신이나 보건 관련 인력을 통해 제공되었습니다. 결과 측정은 임상적 평가, 생화학적 평가, 인체 측정 평가 또는 식이 평가 등 결과의 성격에 따라 다양한 그룹에서 수행되었습니다. 보건 종사자 간부에 대한 더 자세한 설명은 포함된 연구의 특성 에 제시되어 있습니다 .
비타민 D 상태 평가를 위한 실험실 방법론
비타민 D 상태를 혈청 25‐하이드록시비타민 D 농도로 측정하기 위해 다양한 실험실 방법이 사용되었습니다. 5건의 임상시험( Asemi 2012 ; Asemi 2013a ; Sabet 2012 ; Sablok 2015 ; Samimi 2016 )에서는 면역측정 ELISA 키트를 사용하여 측정했습니다. 6건의 시험에서는 화학발광 효소 표지 면역측정 분석법을 사용했습니다( Benson 2009 ; Bhutta 2011 ; Diogenes 2013 ; Harvey 2012 ; Singh 2015 ; Vaziri 2016 ). 또 다른 시험에서는 동위원소 희석 액체 크로마토그래피-직렬 질량 분석법을 사용했습니다( Grant 2013 ). 두 번의 시험에서는 경쟁적 단백질 결합 분석을 사용했습니다( Brooke 1980 ; Mallet 1986 ). 한 실험에서는 방사성 리간드 분석을 사용했습니다( Delvin 1986 ). 두 번의 시험에서는 Liebermann‐Buchard 방법을 사용했습니다( Sasan 2017 ; Shahgheibi 2016 ). 고성능 액체 크로마토그래피 탠덤 질량 분광법(LCMS/MS)을 사용한 시험은 2건뿐이었습니다( Roth 2010 ; Roth 2013 ). 두 번의 시도에서는 실험실 방법이 보고되지 않았습니다( Samimi 2017 ; Yu 2008 ). 다른 임상시험에서는 이 결과를 보고하지 않았습니다( Kaur 1991 ; Li 2000a ; Marya 1987 ; Marya 1988 ; Mazurkevich 2013 ; Mirghafourvand 2013 ; Naghshineh 2016 ; Samimi 2016 ; Tehrani 2014 ).
자금 출처
임상시험은 주로 대학, 보건 기관, 비정부 기관의 연구 보조금으로 자금을 지원받았습니다. 때로는 조합해서. 연구부총장은 Asemi 2012 와 Asemi 2013a를 지원했다 . 호주 및 뉴질랜드 산부인과 대학 연구 재단의 Luke Proposch 주산기 연구 장학금이 Benson 2009를 지원했습니다 . 엄마와 신생아를 위한 파키스탄 이니셔티브(PAIMAN)는 Bhutta 2011을 지원했습니다 . 병리학 연구 기금, 세인트 조지 병원 의과대학 및 남서부 템스 지역 보건 당국이 Brooke 1980 에 자금을 지원했습니다 . 북미의 Shriners, 프랑스-퀘벡 교환 프로그램 및 INSERM이 Delvin 1986 에 자금을 지원했습니다 . Conselho Nacional de Desenvolvimento Cientıfico e Tecnologico와 Fundacao Carlos Chagas Filho de Amparo a` Pesquisa do Estado do Rio de Janeiro는 Diogenes 2013을 지원했습니다 . 뉴질랜드 보건 연구 위원회와 Cure Kids가 Grant 2013을 지원했습니다 . 영국 관절염 연구회(Arthritis Research UK), 의학 연구 위원회(Medical Research Council), Bupa 재단, 국립 보건 연구소(National Institute for Health Research)가 Harvey 2012를 지원했습니다 . Tabriz University of Medical Sciences는 Mirghafourvand 2013에 자금을 지원했습니다 . 이스파한 의과대학은 Naghshineh 2016을 지원했습니다 . Thrasher 연구 기금은 Roth 2010을 지원했고 Bill & Melinda Gates 재단은 Roth 2013을 지원했습니다 . 내분비 과학 연구소와 Shahid Beheshti 의과 대학은 Sabet 2012를 지원했습니다 . Kashan University of Medical Sciences는 Samimi 2016 과 Samimi 2017 에 자금을 지원했습니다 . Isfahan University of Medical Sciences의 연구 부교수는 Taherian 2002를 지원했습니다 . Tehrani 2014에서는 자금 지원을 보고하지 않았습니다. Shiraz University of Medical Sciences의 연구 부총장은 Vaziri 2016을 지원했습니다 . 산부인과 신탁 연구소와 가족 건강을 위한 Wolfson 및 Weston 연구 센터는 Yu 2008을 지원했습니다 . Sablok 2015는 자체 자금을 조달했습니다. Kaur 1991 , Li 2000a , Mallet 1986 , Marya 1987 , Marya 1988 , Mazurkevich 2013 , Sasan 2017 및 Singh 2015 의 경우 자금이 알려지지 않았거나 보고되지 않았습니다. 예를 들어 비타민 D 제조업체 또는 이와 유사한 자금 출처가 있는 임상시험은 없었습니다. Shahgheibi 2016은 자금을 받지 못했다고 보고했습니다.
관심 선언
다음 임상시험에서는 저자 중 어느 누구도 이해 상충이 없다고 보고했습니다. Asemi 2013a ; 벤슨 2009 ; 디오게네스 2013 ; 그랜트 2013 ; 미르가푸르반드 2013 ; 로스 2010 ; 로스 2013 ; 사베트 2012 ; 사블록 2015 ; 사미미 2016 ; 사미미 2017 ; 사산 2017 ; 샤게이비 2016 ; 테헤라니 2014 ; 바지리 2016 .
다음 임상시험에서는 발행물에 이해 상충 설명이 포함되지 않았습니다. Asemi 2012 ; 부타 2011 ; 브룩 1980 ; 델빈 1986 ; 카우르(1991) ; 리2000a ; 말렛 1986 ; 마리아 1987 ; 마리아 1988 ; 마주르케비치 2013 ; 나그샤인 2016 ; 싱 2015 ; 타헤리안 2002 ; 유 2008 .
이해 상충을 보고한 임상시험은 Harvey 2012 뿐입니다 .
사용된 비타민 D 용량 및 비교 요법을 포함하여 임상시험에 대한 자세한 설명은 포함된 연구의 특성을 참조하세요 .
제외된 연구
60개의 임상시험을 제외했습니다. 제외의 주된 이유는 26개 임상시험에서 비타민 D의 다양한 용량을 비교했기 때문입니다( Baqui 2009 ; Bhatia 2012 ; Bhatia 2010 ; Bisgaard 2009 ; Dawodu 2013 ; de Menibus 1984 ; Gerais 2015 ; Hashemipour 2014 ; Kachhawa 2014 ; Kiely 201 ) 5 , Lalooha 2012 , 2010년 3월 , Marya 1981 , McLean 2012 , Mojibian 2015 , Mutlu 2013 , Nausheen 2014 , Rostami 2018 , Shakiba 2013 , Stephensen 2011 , Thiele 2014 , Wagner 2006a , Wagner 200 6b ; Wagner 2013 ; Weiss 2009 ; Yap 2014 ), 위약 없이 또는 치료 조절 없이. 또한 비타민 D 이외의 보충제에 제공된 다른 영양소가 치료 그룹에서 달랐고( Asemi 2015 ; Azami 2017 ; Pandey 2015 ), 1개의 실험에는 비타민 D가 포함된 그룹이 없었기 때문에 3개의 실험은 제외되었습니다( Atkinson 2010 ). 또한 4건의 임상시험은 무작위 임상시험이 아니었습니다( Ala‐Houhala 1986 ; Cockburn 1980 ; Bhatia 2010 ; Ito 1994 ). 4건의 임상시험( Czech‐Kowalska 2013 ; Niramitmahapanya 2017 ; Taheri 2014 ; von Hurst 2009 )이 임신하지 않은 여성을 대상으로 실시되었습니다. 포도당 불내증 또는 임신성 당뇨병이 있는 임산부를 대상으로 12건의 임상시험이 수행되었습니다( Asemi 2013b ; Asemi 2014 ; Jamilian 2016 ; Jamilian 2017 ; Karamali 2014 ; Li 2016 ; Mozzafari 2010 ; Razavi 2017 ; Simsek 2011 ; Valizadeh 2016 ; Yaz dchi 2016 , 장 2016 ) 또는 기타 만성 질환( Etemadifar 2015 ; Shi 2017 ; Sudfeld 2017 ), 1건의 임상시험은 산후 여성에게만 실시되었으며( Chandy 2016 ), 1건의 임상시험은 출산 목적으로 부부를 대상으로 실시되었습니다( Kermack 2017).). 한 참고문헌은 Oxford Database of Perinatal Trials에 1986년에 등록된 임상시험을 언급하고 1979년에 완료된 모집 및 후속 조치를 보고했지만 이용 가능한 보고서가 없었고 해당 임상시험을 등록한 저자를 찾을 수 없었습니다( MacDonald 1986 ) . . 치료 그룹이 비타민 D 보충보다 더 다르기 때문에 한 번의 시험은 제외되었습니다( Hossain 2012 ). 제외 이유와 함께 제외된 임상시험에 대한 자세한 설명은 제외된 연구의 특성을 참조하세요 .
포함된 연구의 비뚤림 위험
배당
시퀀스 생성
우리는 무작위 순서를 생성하기 위한 적절한 방법이 있는 것으로 21개의 시험을 평가했습니다. 10건의 시험에서는 컴퓨터 생성 난수 시퀀스를 사용했으며( Asemi 2013a , Diogenes 2013 , Grant 2013 , Harvey 2012 , Naghshineh 2016 , Roth 2010 , Roth 2013 , Sablok 2015 , Samimi 2016 , Yu 2008 ), 4건은 순열 블록 무작위화를 사용했습니다( Bhutta 2011 ) ; Mirghafourvand 2013 ; Samimi 2017 ; Vaziri 2016 ), 7개의 시험에서는 무작위 숫자 테이블( Asemi 2012 ; Benson 2009 ; Mallet 1986 ; Sasan 2017 ; Shahgheibi 2016 ; Taherian 2002 ; Tehrani 2014 )을 사용하여 개입 그룹을 무작위화했습니다. 다른 시험에서는 시험을 무작위로 보고했지만 서열을 생성하는 데 사용된 방법은 설명되지 않았습니다( Brooke 1980 ; Delvin 1986 ; Kaur 1991 ; Marya 1987 ; Marya 1988 ; Mazurkevich 2013 ; Sabet 2012 ; Singh 2015 ). 한 임상시험에서는 참가자가 치료 그룹에 무작위로 할당되었다는 점을 언급하지 않았습니다( Li 2000a ).
할당 은폐
우리는 13개의 임상시험이 적절한 할당 은폐 방법을 갖고 있다고 판단했다( Asemi 2013a ; Asemi 2012 ; Benson 2009 ; Bhutta 2011 ; Grant 2013 ; Harvey 2012 ; Roth 2010 ; Roth 2013 ; Samimi 2016 ; Samimi 2017 ; Shahgheibi 2016 ; Tehrani 2014 년 , 유 2008년 ). 그룹 중 하나가 보충을 받지 않았기 때문에 다음 실험에서는 할당 은폐가 발생하지 않았다고 가정합니다: Kaur 1991 ; 리2000a ; 말렛 1986 ; 마리아 1987 ; 마리아 1988 ; 마주르케비치 2013 ; 사블록 2015 ; 싱 2015 ; 타헤리안 2002 . Sablok 2015 에서는 중재 복용량이 비타민 D 상태에 따라 달라지므로 기준선에서 비타민 D 상태에 따른 선택 편향이 있었습니다. Harvey 2012 의 경우 , 28주차 참가자들은 혈청 25‐hydroxyvitamin D를 측정했고, 75nmol/L 미만인 경우 복용량을 4000IU로 두 배 늘렸습니다. 다른 사람들은 은폐 방법을 보고하지 않았습니다( Brooke 1980 ; Delvin 1986 ; Diogenes 2013 ; Mirghafourvand 2013 ; Naghshineh 2016 ; Sabet 2012 ; Sasan 2017 ; Vaziri 2016 ).
눈이 멀다
참가자, 직원 및 결과 평가자의 눈을 멀게 함
15개 임상시험의 연구자들은 이중 맹검 설계를 사용했다고 보고했습니다( Asemi 2013a ; Bhutta 2011 ; Brooke 1980 ; Grant 2013 ; Harvey 2012 ; Mirghafourvand 2013 ; Naghshineh 2016 ; Roth 2010 ; Roth 2013 ; Sabet 2012 ; Samimi 201 6, 사 미미 2017 , Sasan 2017 , Shahgheibi 2016 , Tehrani 2014 ). 그러나 10개의 임상시험에서만 참가자와 평가를 수행하는 사람 모두가 눈이 멀었다고 명시했습니다( Asemi 2013a ; Bhutta 2011 ; Grant 2013 ; Harvey 2012 ; Naghshineh 2016 ; Roth 2010 ; Roth 2013 ; Sasan 2017 ; Shahgheibi 2016 ; Tehrani 2014 ). 2건의 임상시험이 참가자에 대해서만 맹검된 단일 맹검으로 보고되었습니다( Asemi 2012 ; Diogenes 2013 ). Vaziri 2016 의 시험에서는 단일 맹검 연구라고 보고했습니다. 그러나 우울증은 맹검 간호사가 평가했지만 나머지 평가는 맹검 직원이 수행한 경우 명확하지 않았습니다. 나머지 시험은 단일 맹검으로 보고되었지만 그룹 중 하나는 보충을 받지 않았기 때문에 참가자가 아닌 평가 팀에 대해 맹검으로 간주되었습니다: Benson 2009 , Delvin 1986 ; 카우르(1991) ; 리2000a ; 말렛 1986 ; 마리아 1987 ; 마리아 1988 ; 마주르케비치 2013 ; 사블록 2015 ; 싱 2015 ; 타헤리안 2002 ; 유 2008 .
불완전한 결과 데이터
16개의 임상시험에는 불완전한 데이터가 없었습니다: Asemi 2012 ; 아세미 2013a ; 그랜트 2013 ; 하비 2012 ; 미르가푸르반드 2013 ; 나그샤인 2016 ; 로스 2010 ; 로스 2013 ; 사베트 2012 ; 사미미 2016 ; 사미미 2017 ; 사산 2017 ; 샤게이비 2016 ; 타헤리안 2002 ; 테헤라니 2014 ; 유 2008 ). 다른 사람들은 감소, 데이터 누락 및 치료 의도 분석 부족에 대해 보고하지 않았습니다.
선택적 보고
우리는 연구 프로토콜에 접근할 수 없었기 때문에 보고 편향을 공식적으로 평가하는 것이 불가능했습니다. 불충분한 시험은 깔때기 도표를 사용하여 출판 편향 가능성을 탐색할 수 있는 데이터를 제공했습니다.
편향의 기타 잠재적인 원인
이는 다양한 실험에서 다양했습니다. 예를 들어, Harvey 2012 에서는 참가자들이 자신의 종합 비타민제를 계속 복용할 수 있다고 보고했지만 연구 중에 누가 그러한 보충제를 복용했는지, 누가 복용하지 않았는지 명시하지 않았습니다. Li 2000a 의 보고서는 매우 짧으며 대부분의 방법 세부 정보를 사용할 수 없습니다. Mallet 1986 의 시험에는 표본 크기가 매우 다른 그룹이 있었습니다. 숫자가 시험을 마친 참가자, 비 무작위 프로세스 또는 무작위 참가자가 개입을 받지 못한 선택 편향을 반영하는지 여부는 불분명합니다. Shagheibi 2016 의 재판에서는 방법에 설명된 것과 초록에서 다른 개입을 보고했습니다.
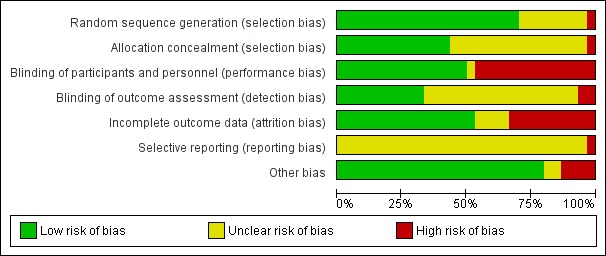
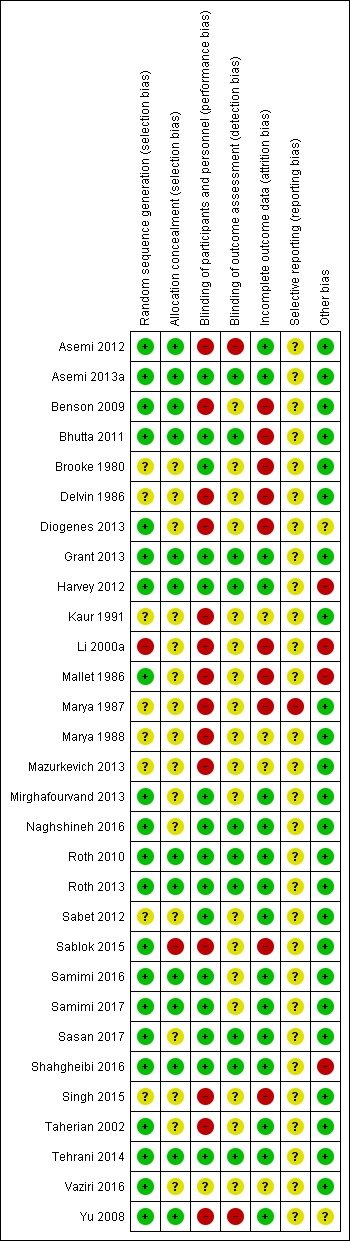
또한 '편향 위험' 평가를 요약한 수치도 포함했습니다(그림 2;그림 3).
개입의 효과
이 업데이트된 검토에는 총 7033명의 여성을 평가하는 30건의 임상시험이 포함되었습니다. 요약 결과를 비교와 1차 및 2차 결과별로 구성했습니다.
데이터 및 분석 표 에서는 미리 지정된 네 가지 비교를 모두 설정했지만 결과 데이터는 이 중 두 가지에만 사용할 수 있었습니다. 데이터가 없는 비교에는 결과를 추가하지 않았습니다(비교 3 및 4). 데이터와의 비교를 위해 우리는 현재 연구 증거의 격차를 강조할 뿐만 아니라 향후 업데이트에서 사용할 수 있는 데이터를 추가할 수 있도록 모든 주요 결과(데이터를 사용할 수 없는 경우에도)에 대한 표를 설정했습니다.
1차 및 2차 결과에 대한 자세한 결과는 데이터 및 분석을 참조하세요 .
각 비교에 대해 데이터를 제공하는 임상시험의 수와 이러한 임상시험에 모집된 총 여성 수를 표시했습니다. 그러나 일부 결과의 경우 1~2건의 임상시험만이 데이터를 제공했으며 후속 조치의 손실로 인해 특정 결과의 분모가 무작위 표본보다 상당히 작을 수 있습니다. 따라서 우리는 데이터를 제공하는 임상시험의 수와 해당 분석에 포함된 여성의 수를 표시했습니다.
(1) 비타민 D 단독 보충 대 위약 또는 개입 없음(비타민이나 미네랄 없음)(22건의 임상시험, 3,725명의 여성)
이 비교에는 3,725명의 임산부를 대상으로 한 22건의 임상시험이 포함되었습니다( Asemi 2013a ; Benson 2009 ; Bhutta 2011 ; Brooke 1980 ; Delvin 1986 ; Grant 2013 ; Harvey 2012 ; Kaur 1991 ; Mallet 1986 ; Marya 1988 ; Mirghafourvand 2013 ; 나그샤인 2016 ; Roth 2010 , Sabet 2012 , Sablok 2015 , Samimi 2017 , Sasan 2017 , Shahgheibi 2016 , Singh 2015 , Tehrani 2014 , Vaziri 2016 , Yu 2008 ). 두 번의 시험이 비교 1과 2 모두에 기여했습니다( Asemi 2013a ; Mirghafourvand 2013 ).
다음 시험은 할당 및 눈가림에 대한 비뚤림 위험이 낮은 것으로 평가되었습니다: Asemi 2013a ; 부타 2011 ; 그랜트 2013 ; 하비 2012 ; 미르가푸르반드 2013 ; 나그샤인 2016 ; 로스 2010 ; 사미미 2017 ; 샤게이비 2016 ; 테헤라니 2014 . 다음 임상시험은 할당 및 눈가림에 대한 비뚤림 위험이 높은 것으로 평가되었습니다: Delvin 1986 ; 카우르(1991) ; 말렛 1986 ; 마리아 1988 ; 사블록 2015 ; 싱 2015 . Benson 2009 및 Yu 2008은 실명 위험이 높았습니다. Sabet 2012는 무작위 순서 생성이나 결과 평가의 맹검에 대해 보고하지 않았습니다. Brooke 1980 과 Vaziri 2016은 이러한 문제의 대부분을 보고하지 않았기 때문에 편견의 위험을 판단할 수 없었습니다. Sasan 2017 에서는 할당 은폐가 잘 설명되지 않아 편향 위험이 불분명한 것으로 평가되었습니다.
주요 결과
산모
자간전증(시험의가 정의한 대로)
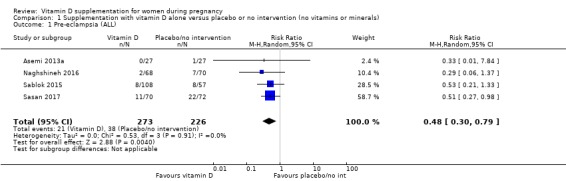
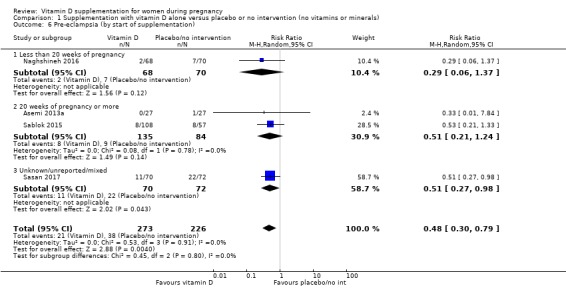
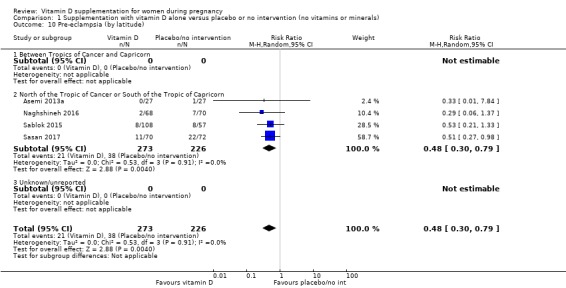
499명의 여성을 대상으로 한 4건의 임상시험( Asemi 2013a ; Naghshineh 2016 ; Sablok 2015 ; Sasan 2017 )에서 나온 데이터에 따르면 비타민 D 보충은 중재가 없거나 위약에 비해 자간전증의 위험을 줄일 수 있는 것으로 나타났습니다(위험 비율(RR 0.48, 95% CI) 0.30 ~ 0.79), 중간 정도의 근거 확실성 ,분석 1.1). Sablok 2015 의 데이터는 전자간증과 임신성 고혈압에 대한 데이터를 함께 포함했기 때문에 이전 업데이트( De‐Regil 2016 )에 잘못 입력되었습니다. 저자에게 연락했고 이제 자간전증에 대한 데이터만 여기에 보고되고 임신성 고혈압에 대한 데이터가 해당 결과에 보고됩니다. Sasan 2017 임상시험에 참여한 모든 여성이 자간전증의 병력이 있었다는 점에 유의하는 것도 중요합니다 .
임신성 당뇨병(시험의자가 정의한 대로)
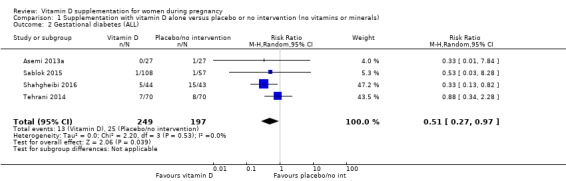
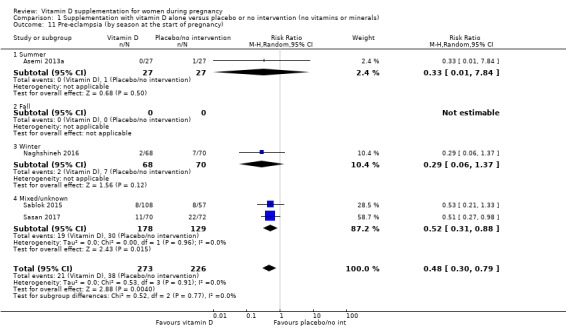
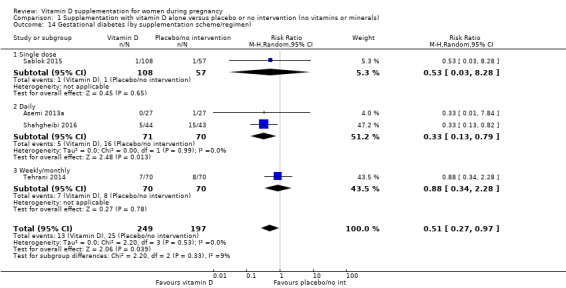
446명의 여성을 대상으로 한 4건의 임상시험( Asemi 2013a ; Tehrani 2014 ; Naghshineh 2016 ; Sablok 2015 )의 데이터에 따르면 비타민 D 보충은 중재를 받지 않은 여성이나 위약군(RR 0.51, 95)에 비해 임신성 당뇨병 위험을 줄일 수 있는 것으로 나타났습니다. % CI 0.27~0.97, 중간 정도의 근거 확실성,분석 1.2).
산모 부작용 분석 1.3
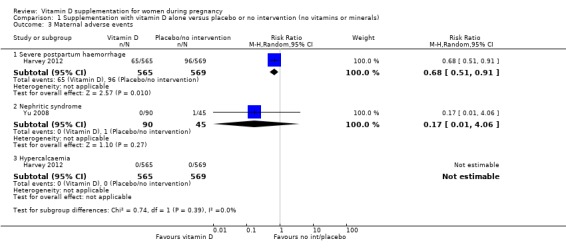
1건의 임상시험에서는 1,134명의 여성을 대상으로 심각한 산후 출혈이 보고되었습니다( Harvey 2012 ). 비타민 D 보충은 심각한 산후 출혈 위험을 감소시키는 것으로 보이지만(RR 0.68, 95% CI 0.51 ~ 0.91; 1건의 임상시험, 1134명의 여성, 낮은 근거 확실성 ), 이 결과는 단일 임상시험에 기초한 것이며 다른 어떤 연구에서도 이전에 문서화되지 않은 예상치 못한 발견이었습니다. 135명의 여성을 대상으로 한 신염 증후군에 대해 보고된 또 다른 시험( Yu 2008 ); 그룹 간에 명확한 차이는 발견되지 않았습니다(대조군에서는 단 하나의 사건: RR 0.17, 95% CI 0.01 ~ 4.06, 매우 낮은 근거 확실성 ). 고칼슘혈증과 관련하여 단 한 번의 시험에서만 이 결과가 보고되었으며( Harvey 2012 ) 어떤 그룹에서도 고칼슘혈증이 발생한 사례는 없었습니다. 산모의 이상반응에 대한 일반적인 데이터가 부족하기 때문에 확고한 결론을 내릴 수는 없습니다.
유아
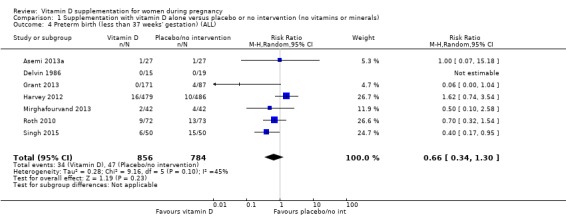
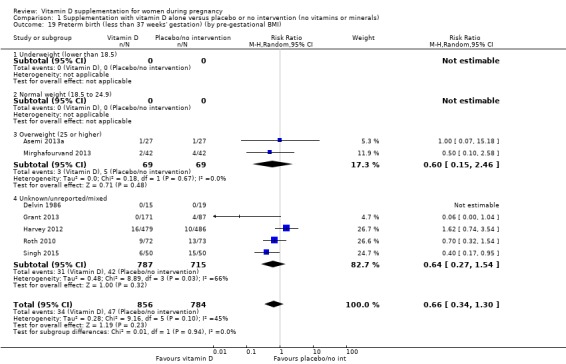
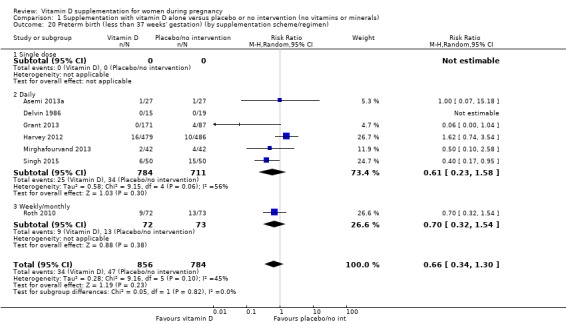
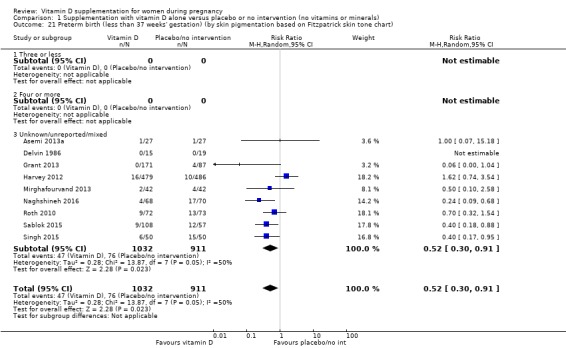
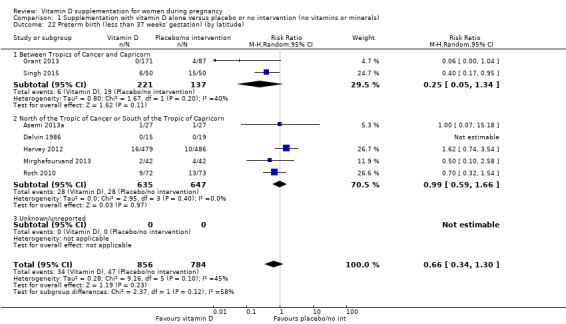
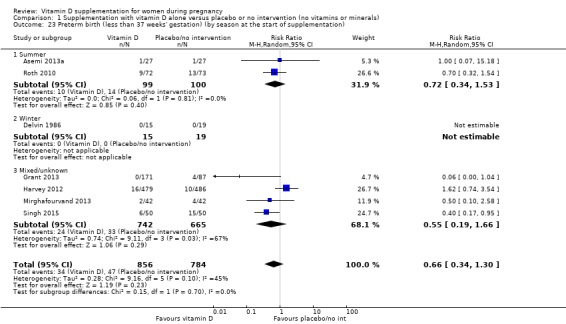
조산(임신 기간 37주 미만)
1,640명의 여성을 대상으로 한 7건의 임상시험( Asemi 2013a ; Delvin 1986 ; Harvey 2012 ; Grant 2013 ; Mirghafourvand 2013 ; Roth 2010 ; Singh 2015 )의 데이터에 따르면 비타민 D 보충은 조산 위험에 거의 또는 전혀 차이가 없을 수 있습니다. 중재 없음 또는 위약과 비교(RR 0.66, 95% CI 0.34 ~ 1.30, 낮은 확실성 근거 ;분석 1.4). Singh(2015) 에서는 중재 그룹의 참가자가 대조군에 비해 기준선에서 25‐hydroxyvitamin D 수준이 상당히 낮았으므로 연구 그룹에 불균형이 있었다는 점에 유의하는 것이 중요합니다 . 그러나 이 임상시험에서 조산 위험을 낮추는 결과는 다른 임상시험과 일치했습니다.
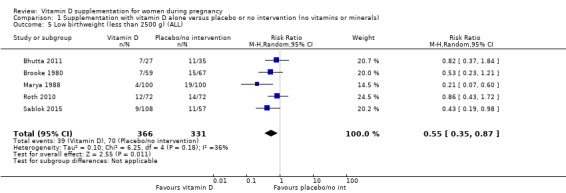
저체중 출생(2500g 미만)
697명의 여성을 대상으로 한 5건의 임상시험( Brooke 1980 ; Bhutta 2011 ; Marya 1988 ; Roth 2010 ; Sablok 2015 )에서 나온 데이터는 비타민 D 보충이 중재가 없거나 위약(RR)에 비해 저체중 출생(< 2500g)의 위험을 줄일 수 있음을 시사합니다. 0.55, 95% CI 0.35 ~ 0.87, 중간 정도의 근거 확실성,분석 1.5).
하위그룹 분석
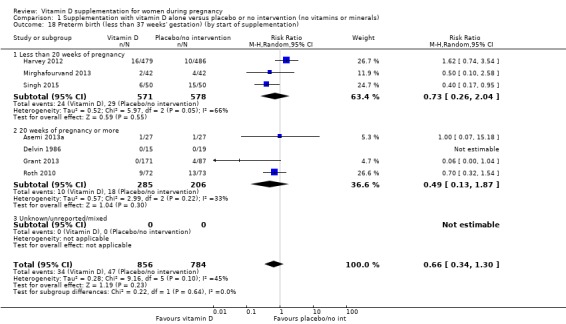
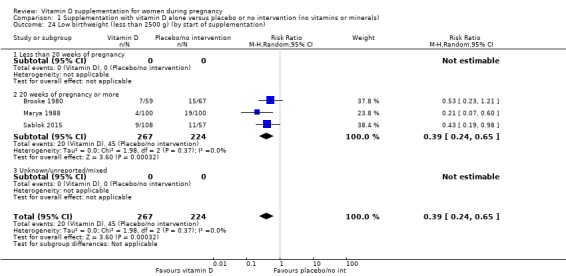
조산의 경우, 임신 20주차 이전에 보충을 시작했는지(3건의 임상시험, 여성 1,149명)(RR 0.73, 95% CI 0.26~2.04), 임신 20주 이후에(4건의 임상시험, 491명의 여성) 결과는 크게 다르지 않았습니다. RR 0.49, 95% CI 0.13~1.87;분석 1.18).
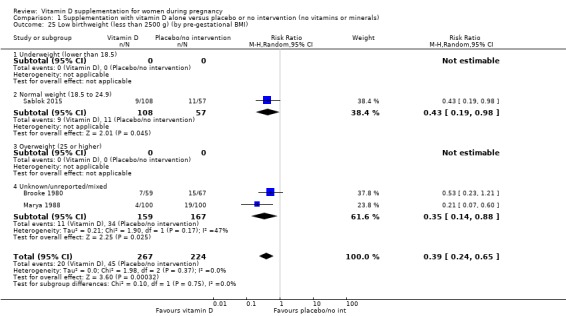
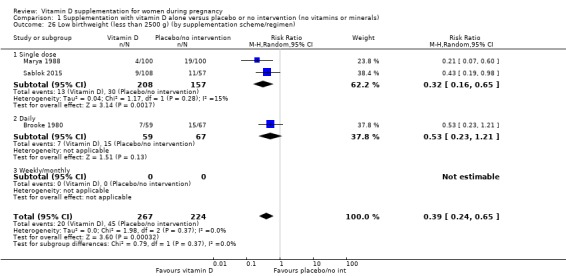
다른 하위 그룹 분석과 관련하여 대부분은 1~2번의 시도만 수행했습니다(분석 1.6,분석 1.7;분석 1.8;분석 1.9;분석 1.10;분석 1.11;분석 1.12;분석 1.13;분석 1.14;분석 1.15;분석 1.16;분석 1.17;분석 1.19;분석 1.20;분석 1.21;분석 1.22;분석 1.23;분석 1.24;분석 1.25;분석 1.26;분석 1.27;분석 1.28;분석 1.29).
2차 결과
산모
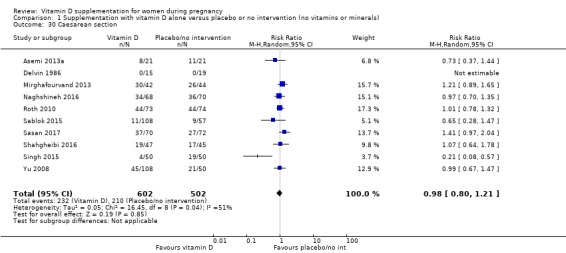
제왕 절개
1,104명의 여성을 포함한 10건의 임상시험이 이 결과에 대해 보고했습니다( Asemi 2013a ; Delvin 1986 ; Mirghafourvand 2013 ; Naghshineh 2016 ; Roth 2010 ; Sablok 2015 ; Sasan 2017 ; Shahgheibi 2016 ; Singh 2015 ; Yu 2008 ). 이 시험의 데이터에 따르면 비타민 D 보충은 보충하지 않거나 위약에 비해 제왕절개 위험에 거의 또는 전혀 차이가 없는 것으로 나타났습니다(RR 0.98, 95% CI 0.80 ~ 1.21;분석 1.30). Singh 의 2015년 시험은 중재를 통해 제왕절개 위험이 더 낮다는 것을 확인한 유일한 시험이었습니다. 그러나 중재 그룹의 참가자들은 대조군에 비해 기준선에서 25‐hydroxyvitamin D 수준이 현저히 낮았기 때문에 불균형이 있었습니다. 스터디 그룹. 이 시험을 분석에서 제외해도 결과는 변경되지 않았습니다(RR 1.06, 95% CI 0.93~1.21).
임신성 고혈압
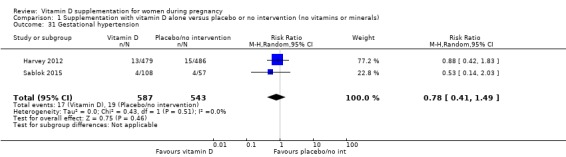
1,130명의 여성을 대상으로 한 이 결과에 대한 두 번의 임상시험이 보고되었습니다( Harvey 2012 ; Sablok 2015 ). 비타민 D 보충은 중재가 없거나 위약에 비해 임신성 고혈압 위험에 거의 또는 전혀 차이가 없을 것입니다(RR 0.78, 95% CI 0.41~1.49;분석 1.31).
내당능 장애
어떤 임상시험도 이 결과를 보고하지 않았습니다.
만삭 시 산모의 비타민 D 농도(nmol/L 단위로 25‐하이드록시비타민 D)
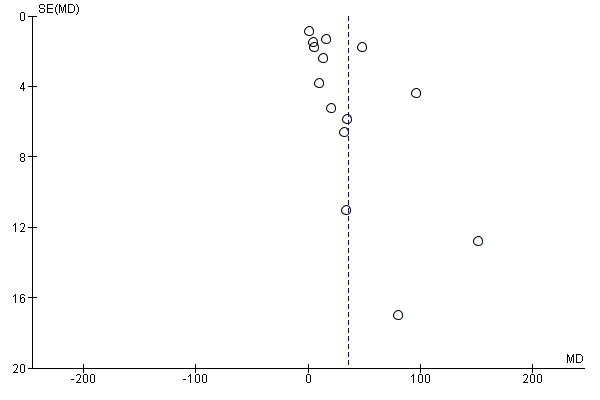
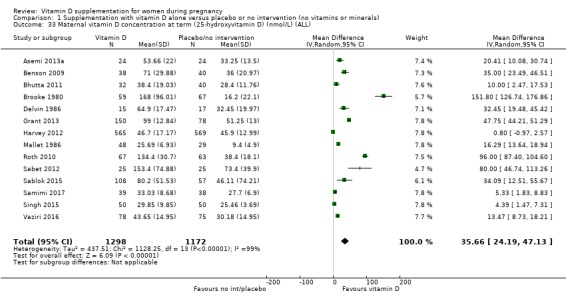
14개 임상시험의 데이터( Asemi 2013a , Benson 2009 , Bhutta 2011 , Brooke 1980 , Delvin 1986 , Grant 2013 , Harvey 2012 , Mallet 1986 , Roth 2010 , Sabet 2012 , Sablok 2015 , Samimi 2017 , Singh 2) 015 ; Vaziri 2016 ) 2470 관련 여성은 비타민 D 보충이 중재를 받지 않거나 위약을 받은 여성보다 25‐hydroxyvitamin D 농도가 더 높아질 가능성이 있음을 보여줍니다. 그룹 간 평균 평균 차이(MD)는 35.66nmol, 리터당 25‐하이드록시비타민 D(95% CI 24.19~47.13;분석 1.33). 이 결과는 보충에 대한 반응이 매우 이질적이었고(Tau² = 437.5, I² = 99% 및 이질성에 대한 Chi² 테스트 P < 0.00001) 범위가 리터당 16.3nmol 25‐히드록시비타민 D(95% CI 13.6 ~ 19.0)였으므로 주의 깊게 해석해야 합니다. ) ( Mallet 1986 ) ~ 152 nmol 리터당 25‐하이드록시비타민 D (95% CI 127 ~ 177) ( Brooke 1980 ). Brooke 1980 의 시도가 제거되더라도 이질성은 유사하게 유지됩니다. Singh 2015 의 시험에서는 기준선에서 이 결과에 연구 그룹에 불균형이 있었음에도 불구하고 다른 시험과 일관된 결과를 발견했습니다. 그러나 결과는 실험 간에 일관되게 나타났습니다. 우리는 또한 이 결과에서 깔때기 도표의 비대칭성을 발견했습니다(그림 4); 깔때기 플롯 비대칭이 존재한다는 것은 출판 편향이 이러한 이질성의 원인일 가능성이 있음을 시사했습니다.
유아
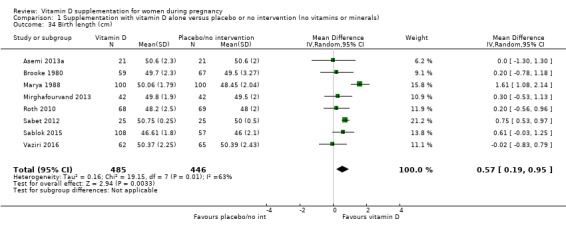
출생 시 길이(cm)
931명의 여성을 대상으로 한 8건의 임상시험( Asemi 2013a ; Brooke 1980 ; Marya 1988 ; Mirghafourvand 2013 ; Roth 2010 ; Sabet 2012 ; Sablok 2015 ; Vaziri 2016 )에서 얻은 데이터는 아마도 임신 중에 비타민 D 보충제를 복용하는 여성에게서 태어난 영아의 출생 기간이 더 길다는 것을 시사합니다. 무치료군 또는 위약군 여성(MD 0.57, 95% CI 0.19~0.95;분석 1.34). 보충에 대한 반응에는 이질성이 있었고(Tau² = 0.16; I² = 63% 및 이질성에 대한 Chi² 테스트 P = 0.008) 이러한 연구의 대부분은 결과 평가가 눈이 먼 사람에 의해 수행되었는지 보고하지 않았습니다( Brooke 1980 ; Marya 1988 ; Mirghafourvand 2013 , Sabet 2012 , Sablok 2015 , Vaziri 2016 ). 이를 고려하고 효과가 매우 작다는 점을 고려하면 이러한 결과는 주의해서 해석되어야 합니다.
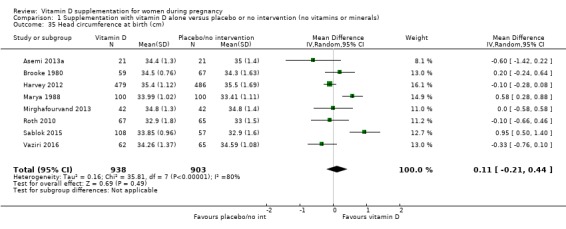
출생 시 머리둘레(cm)
1,841명의 여성을 대상으로 한 8건의 임상시험( Asemi 2013a ; Brooke 1980 ; Harvey 2012 ; Marya 1988 ; Mirghafourvand 2013 ; Roth 2010 ; Sablok 2015 ; Vaziri 2016 )에서 이러한 인체 측정 결과가 보고되었습니다. 결과는 비타민 D 보충이 치료를 받지 않은 경우나 위약에 비해 출생 시 머리 둘레에 거의 또는 전혀 차이가 없는 것으로 나타났습니다(MD 0.11, 95% CI ‐0.21 ~ 0.44;분석 1.35). 보충에 대한 반응에는 이질성이 있었습니다(Tau² = 0.16; I² = 80% 및 이질성에 대한 Chi² 테스트 P < 0.00001). 따라서 결과를 주의해서 해석해야 합니다.
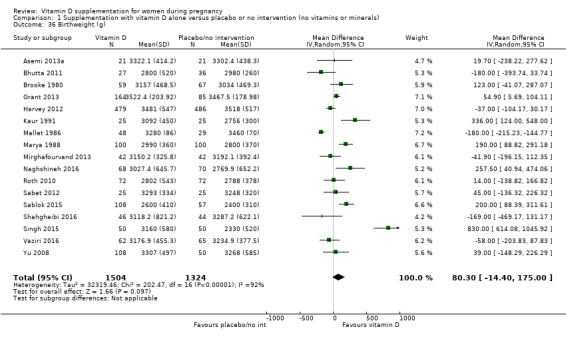
출생 체중(g)
2,828명의 여성이 참여한 17건의 임상시험( Asemi 2013a ; Bhutta 2011 ; Brooke 1980 ; Grant 2013 ; Harvey 2012 ; Kaur 1991 ; Mallet 1986 ; Marya 1988 ; Mirghafourvand 2013 ; Naghshineh 2016 ; Roth 2010 ; Sabet 201 2 , Sablok 2015 , Shahgheibi 2016 , Singh 2015 ; Vaziri 2016 ; Yu 2008 )이 이 결과를 보고했습니다. 결과는 비타민 D 보충이 치료를 받지 않거나 위약에 비해 출생 체중에 거의 또는 전혀 차이가 없는 것으로 나타났습니다(MD 80.30, 95% CI ‐14.40 ~ 175.00;분석 1.36). 치료 규모 측면에서 시험 간에 상당한 이질성이 있었습니다(Tau² = 32319; I² = 92% 및 이질성에 대한 Chi² 테스트 P < 0.00001). 그러나 Mallet 1986 의 시험을 분석에서 제외하면 이질성이 92%에서 84%로 감소하고 결과에 따르면 비타민 D 보충으로 인해 출생 체중이 더 높아질 수 있습니다(MD 99.27, 95% CI 16.22~182.32). 본 연구의 표준 편차는 매우 작으므로 정확하게 보고되지 않을 수 있다는 우려가 있습니다. 또한 Singh 의 2015년 시험 에서는 다른 시험과 비교하여 매우 다른 결과가 발견되었으며 이는 중재 그룹의 여성이 대조군에 비해 기준선에서 25‐hydroxyvitamin D 수준이 현저히 낮다는 사실로 설명될 수 있습니다. 이 시험도 분석에서 제외되면 이질성은 67%로 더욱 감소하고 그룹 간 유의미한 차이는 없습니다(MD 59.24, 95% CI ‐1.93~120.42).
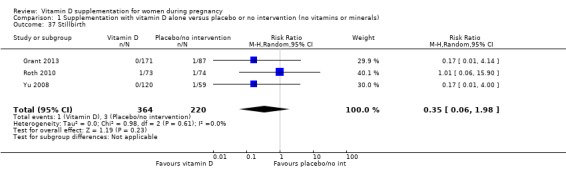
사산(시험 참가자가 정의한 대로)
584명의 여성을 대상으로 한 3건의 임상시험( Grant 2013 ; Roth 2010 ; Yu 2008 )에서 이러한 결과가 보고되었습니다. 비타민 D 보충은 중재가 없거나 위약에 비해 사산 위험에 거의 또는 전혀 차이가 없을 것입니다(RR 0.35, 95% CI 0.06 ~ 1.98;분석 1.37). 특히 이 결과에 대해 비타민 D군에서는 364명 중 1명만이 사산한 것으로 보고됐고, 무개입군이나 위약군에서는 220명 중 3명만 사산한 것으로 나타났다.
신생아 사망(분만 후 28일 이내)
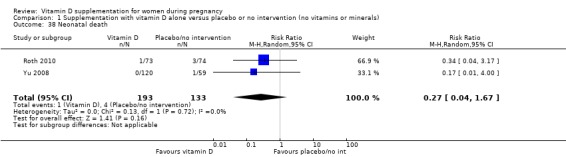
326명의 여성을 대상으로 한 2건의 임상시험( Roth 2010 ; Yu 2008 )에서 이러한 결과가 보고되었습니다. 비타민 D 보충은 중재가 없거나 위약에 비해 신생아 사망 위험에 거의 또는 전혀 차이가 없을 것입니다(RR 0.27, 95% CI 0.04~1.67;분석 1.38). 비타민 D 그룹에서는 193명 중 1명의 신생아 사망만이 보고되었으며, 무개입 또는 위약 그룹에서는 133명 중 4명의 신생아 사망이 보고되었습니다. 이 결과에 대한 데이터가 부족하기 때문에 확실한 결론을 내릴 수는 없습니다.
5분에 아프가 점수가 7 미만
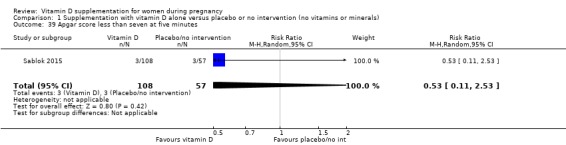
165명의 여성을 포함한 한 연구에서는 그룹 간 Apgar 점수의 명확한 차이를 발견하지 못했습니다(RR 0.53, 95% CI 0.11 ~ 2.53;분석 1.39).
기타 유아 이차 결과
사전 지정된 기타 영아 2차 결과에 대해 보고된 임상시험은 없습니다: 신생아 기간(분만 후 28일 이내) 동안 특별 치료(집중 치료 포함) 입원; 신생아 감염(예: 호흡기 감염) 또는 조기 출산(임신 기간 34주 미만).
(2) 비타민 D + 칼슘 보충 대 위약/무개입(비타민이나 미네랄 없음)(9건의 임상시험, 1916명의 여성)
1916명의 여성을 대상으로 한 9건의 임상시험에서 이러한 비교가 이루어졌습니다( Asemi 2012 ; Asemi 2013a ; Diogenes 2013 ; Li 2000a ; Marya 1987 ; Mazurkevich 2013 ; Mirghafourvand 2013 ; Samimi 2016 ; Taherian 2002 ).
다음 시험은 할당 및 눈가림에 대한 비뚤림 위험이 낮은 것으로 평가되었습니다: Asemi 2013a ; 미르가푸르반드 2013 ; Samimi 2016 , 4개의 임상시험은 비뚤림 위험이 높은 것으로 평가되었습니다: Diogenes 2013 ; 리2000a ; 마리아 1987 ; 마주르케비치 2013 . 나머지 2건의 임상시험에서는 일부 구성 요소의 위험도가 낮거나 위험도가 높거나 위험도가 불명확한 등 혼합된 결과가 나왔습니다. Asemi 2012 ; 타헤리안 2002 .
주요 결과
산모
자간전증(시험의가 정의한 대로)
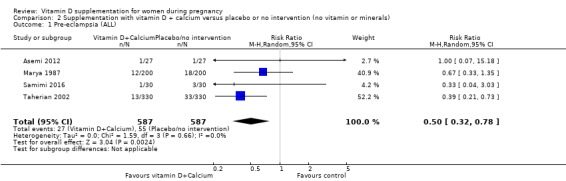
1,174명의 여성을 포함한 4건의 임상시험( Asemi 2012 ; Marya 1987 ; Samimi 2016 ; Taherian 2002 )이 이 결과에 대해 보고했습니다. 비타민 D 보충은 중재가 없거나 위약에 비해 자간전증의 위험을 감소시킬 수 있습니다(RR 0.50, 95% CI 0.32 ~ 0.78; 근거 확실성 중간 ;분석 2.1).
임신성 당뇨병(시험의자가 정의한 대로)
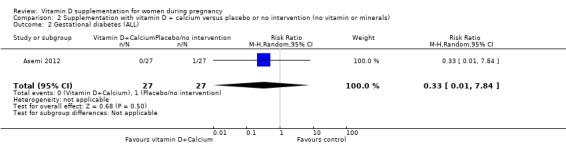
54명의 여성을 포함한 단일 연구에서 이 결과가 보고되었습니다( Asemi 2012 ). 비타민 D 보충이 개입이 없거나 위약에 비해 임신성 당뇨병 위험에 어떤 차이가 있는지는 불확실합니다(RR 0.33, 95% CI 0.01 ~ 7.84; 매우 낮은 근거 확실성 ;분석 2.2). 이 결과에 대한 데이터가 부족하고 CI가 넓기 때문에 확실한 결론을 내릴 수 없습니다.
산모의 부작용
어떤 임상시험도 이 결과를 보고하지 않았습니다.
유아
조산(임신 기간 37주 미만)
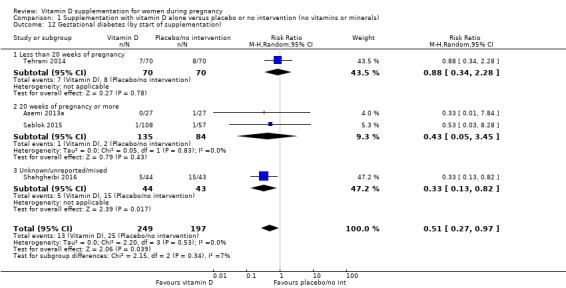
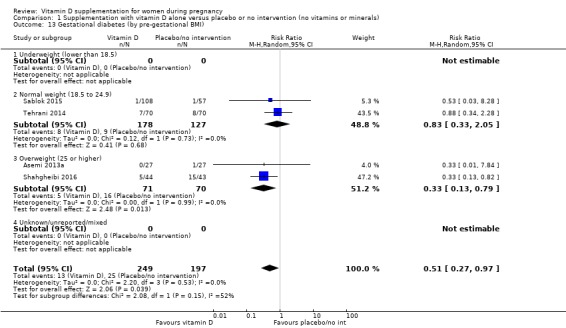
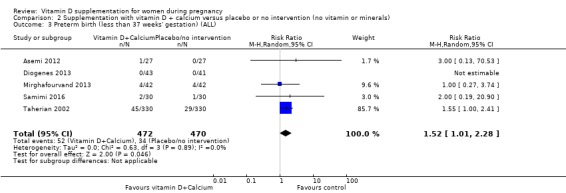
942명의 여성을 대상으로 한 5건의 임상시험에서 이 결과가 보고되었습니다( Asemi 2012 ; Diogenes 2013 ; Mirghafourvand 2013 ; Samimi 2016 ; Taherian 2002 ). 비타민 D 보충은 중재가 없거나 위약에 비해 조산 위험을 증가시킬 수 있습니다(RR 1.52, 95% CI 1.01 ~ 2.28; 근거 확실성 낮음 ;분석 2.3). 이러한 결과는 대부분 대부분의 환자를 모집하고 대부분의 사건이 발생한 한 번의 시험에 의해 주도되었습니다( Taherian 2002 ).
저체중 출생(2500g 미만)
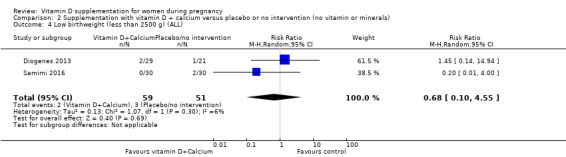
110명의 여성을 대상으로 한 2건의 임상시험에서 이 결과가 보고되었습니다( Diogenes 2013 ; Samimi 2016 ). 비타민 D 보충이 중재가 없거나 위약에 비해 저체중 출생 위험에 어떤 차이가 있는지 불확실합니다(RR 0.68, 95% CI 0.10 ~ 4.55; 매우 낮은 확실성 근거 ;분석 2.4). 이 결과와 CI 전반에 대한 데이터가 부족하여 확실한 결론을 내릴 수 없습니다.
2차 결과
산모
내당능 장애
어떤 임상시험도 이 결과를 보고하지 않았습니다.
제왕 절개
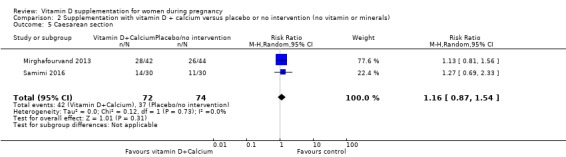
146명의 여성을 포함한 2건의 임상시험에서 이 결과가 보고되었습니다( Mirghafourvand 2013 ; Samimi 2016 ). 비타민 D 보충은 중재가 없거나 위약에 비해 제왕절개 위험에 거의 또는 전혀 차이가 없을 것입니다(RR 1.16, 95% CI 0.87~1.54;분석 2.5).
임신성 고혈압
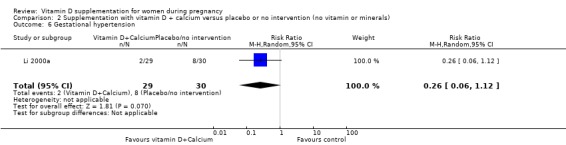
한 임상시험에서는 59명의 여성을 대상으로 이 결과를 보고했습니다( Li 2000a ). 비타민 D 보충은 중재가 없거나 위약에 비해 임신성 고혈압 위험에 거의 또는 전혀 차이가 없을 것입니다(RR 0.26, 95% CI 0.06~1.12;분석 2.6).
모성 사망
어떤 임상시험도 이 결과를 보고하지 않았습니다.
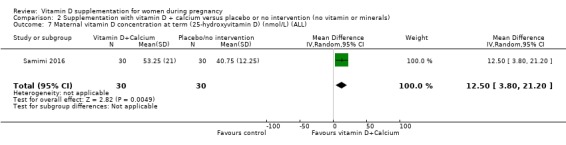
만삭 시 산모의 비타민 D 수치(nmol/L 단위로 25‐하이드록시비타민 D)
60명의 여성을 포함한 단일 연구에서 이 결과가 보고되었습니다( Samimi 2016 ). 그룹 간 평균 MD는 리터당 12.50nmol 25‐하이드록시비타민 D였습니다(95% CI 3.80~21.20;분석 2.7), 그러나 이 결과에 대한 데이터가 부족하고 CI가 광범위하기 때문에 확실한 결론을 내릴 수는 없습니다.
유아
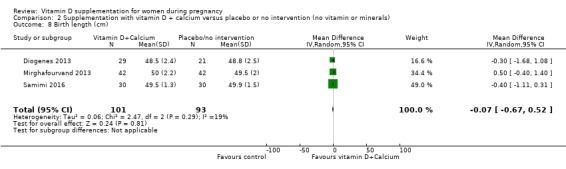
출생 시 길이(cm)
194명의 여성을 대상으로 한 3건의 임상시험( Diogenes 2013 ; Mirghafourvand 2013 ; Samimi 2016 ) 의 데이터에 따르면 비타민 D 보충은 중재가 없거나 위약에 비해 출산 기간에 거의 또는 전혀 차이가 없는 것으로 나타났습니다(MD ‐0.07, 95% CI ‐0.67 ~ 0.52). ;분석 2.8).
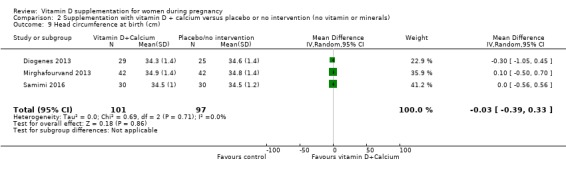
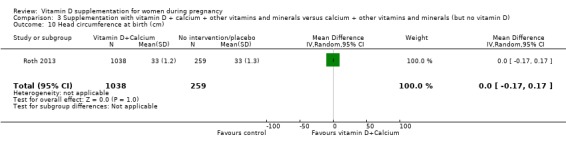
출생 시 머리둘레(cm)
198명의 여성을 대상으로 한 3건의 임상시험( Diogenes 2013 ; Mirghafourvand 2013 ; Samimi 2016 )에서 이러한 인체 측정 결과가 보고되었습니다. 비타민 D 보충은 아마도 중재가 없거나 위약에 비해 출생 시 머리 둘레에 거의 또는 전혀 차이가 없을 것입니다(MD ‐0.03, 95% CI ‐0.39 ~ 0.33;분석 2.9).
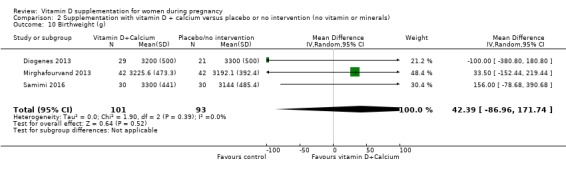
출생 체중(g)
194명의 여성을 대상으로 한 3건의 임상시험( Diogenes 2013 ; Mirghafourvand 2013 ; Samimi 2016 )에서 이 결과가 보고되었습니다. 비타민 D 보충은 중재가 없거나 위약에 비해 출생 체중에 거의 또는 전혀 차이가 없을 것입니다(MD 42.39, 95% CI ‐86.96 ~ 171.74;분석 2.10).
신생아 사망(분만 후 28일 이내)
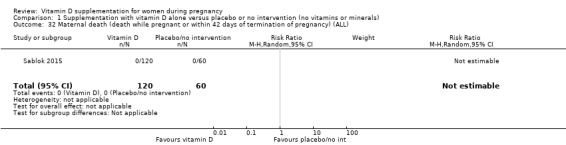
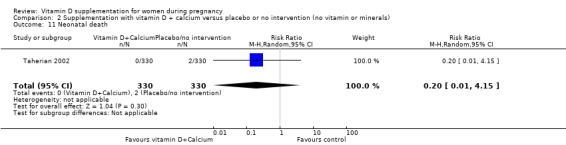
한 연구( Taherian 2002 )에서는 연구 기간 동안 무개입군 또는 위약군(RR 0.20, 95% 0.01 ~ 4.15; 1개 연구, 660명의 여성;분석 2.11).
기타 유아 이차 결과
사전 지정된 기타 영아 2차 결과에 대해 보고된 임상시험은 없습니다: 출생 시 신장(cm); 출생 시 머리 둘레(cm); 출생 시 체중(g); 신생아 기간(분만 후 28일 이내) 동안 특별 치료(집중 치료 포함) 입원, 사산(시험 참가자가 정의한 대로); Apgar 점수는 5분에 7 미만입니다. 신생아 감염(예: 호흡기 감염) 또는 조기 출산(임신 기간 34주 미만).
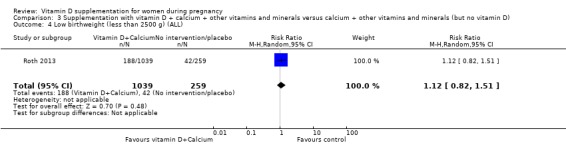
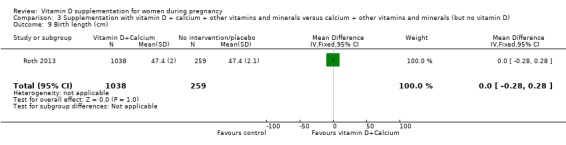
(3) 비타민 D + 칼슘 + 기타 비타민 및 미네랄 보충 대 칼슘 + 기타 비타민 및 미네랄(그러나 비타민 D는 없음)(1개 연구, 1300명의 여성)
이 비교에는 1건의 임상시험이 포함되었습니다( Roth 2013 ). 비뚤림 위험이 낮은 것으로 평가되었습니다.
주요 결과
산모
자간전증(시험의가 정의한 대로)
이 비교에 포함된 연구에서는 이 결과를 보고하지 않았습니다.
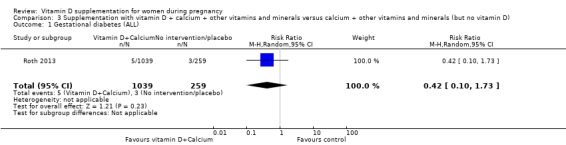
임신성 당뇨병(시험의자가 정의한 대로)
칼슘, 기타 비타민 및 미네랄을 포함한 비타민 D 보충이 중재가 없거나 위약에 비해 임신성 당뇨병 위험에 어떤 차이가 있는지 여부는 불분명합니다(RR 0.42, 95% CI 0.10 ~ 1.73; 1회 시험, 1298명의 여성; 매우 낮은 확실성 증거;분석 3.1) 근거의 확실성이 매우 낮은 것으로 나타났기 때문입니다.
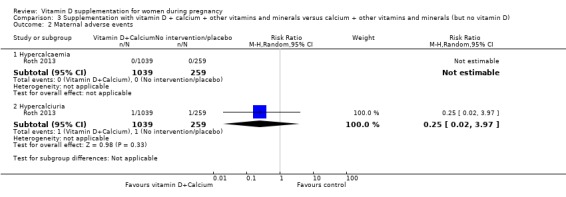
산모의 부작용
칼슘, 기타 비타민 및 미네랄을 포함한 비타민 D 보충이 중재가 없거나 위약과 비교하여 산모의 고칼슘뇨증(확정된 사례) 위험에 어떤 차이가 있는지 여부는 불분명합니다(RR 0.25, 95% CI 0.02 ~ 3.97; 1회 시험, 여성 1298명; 매우 낮은 확실성 근거;분석 3.2) 근거의 확실성이 매우 낮은 것으로 나타났기 때문입니다. 산모의 고칼슘혈증에 대해 확인된 사례는 보고되지 않았습니다.
2차 결과
산모
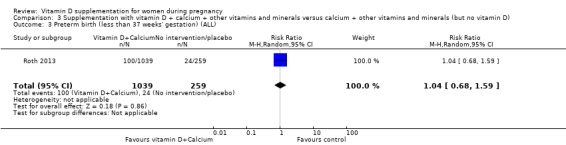
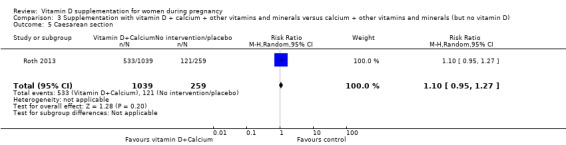
제왕 절개
비타민 D 보충은 중재가 없거나 위약에 비해 제왕절개 위험에 거의 또는 전혀 차이가 없을 것입니다(RR 1.10, 95% CI 0.95 ~ 1.27; 1회 시험, 1298명의 여성;분석 3.5).
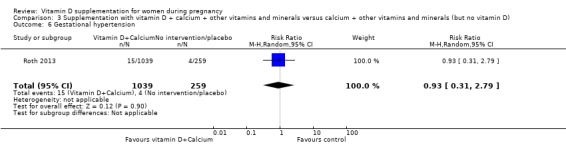
임신성 고혈압
비타민 D 보충은 중재가 없거나 위약에 비해 임신성 고혈압 위험에 거의 또는 전혀 차이가 없을 것입니다(RR 0.93, 95% CI 0.31 ~ 2.79; 1회 시험, 1298명의 여성;분석 3.6).
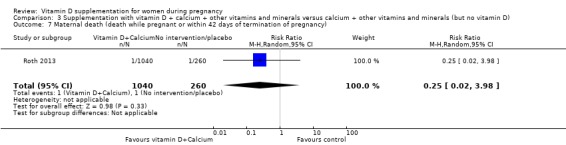
모성 사망
비타민 D 보충은 아마도 중재가 없거나 위약에 비해 산모 사망 위험에 거의 또는 전혀 차이가 없을 것입니다(RR 0.25, 95% CI 0.02 ~ 3.98; 1회 시험, 1300명의 여성;분석 3.7). 비타민 D 그룹에서는 1040명 중 1명의 산모 사망만이 보고되었으며, 무개입 또는 위약 그룹에서는 260명 중 1명의 산모 사망이 보고되었습니다. 이 결과에 대한 데이터가 부족하기 때문에 확실한 결론을 내릴 수는 없습니다.
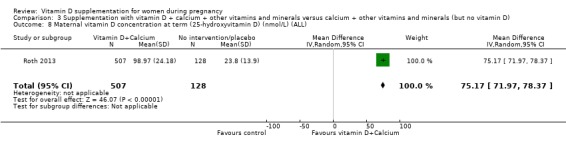
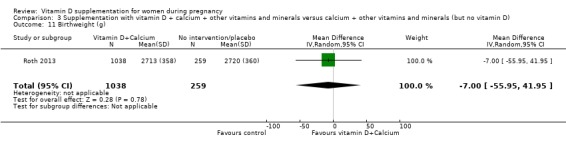
만삭 시 산모의 비타민 D 농도(nmol/L 단위로 25‐하이드록시비타민 D)
그룹 간 평균 MD는 75.17nmol, 리터당 25‐하이드록시비타민 D였습니다(95% CI 71.97~78.37; 1회 시험, 635명의 여성;분석 3.8) 그러나 이 결과에 대한 데이터가 부족하고 CI가 광범위하기 때문에 확실한 결론을 내릴 수는 없습니다.
유아
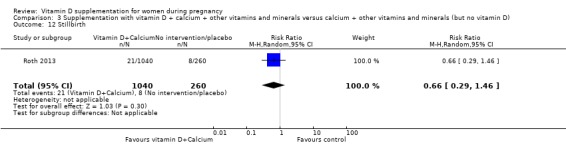
사산(시험 참가자가 정의한 대로)
비타민 D 보충은 아마도 중재가 없거나 위약에 비해 사산 위험에 거의 또는 전혀 차이가 없을 것입니다(RR 0.66, 95% CI 0.29 ~ 1.46; 1회 시험, 1300명의 여성;분석 3.12). 비타민 D 그룹에서는 총 1040명 중 21명의 사산이 보고되었으며, 무개입 또는 위약 그룹에서는 260명 중 8명의 사산이 보고되었습니다. 이 결과에 대한 데이터가 부족하기 때문에 확실한 결론을 내릴 수는 없습니다.
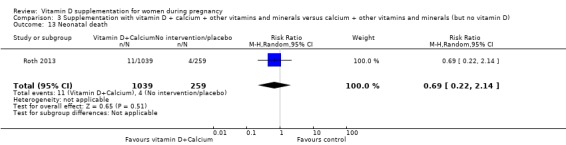
신생아 사망(분만 후 28일 이내)
비타민 D 보충은 아마도 중재가 없거나 위약에 비해 신생아 사망 위험에 거의 또는 전혀 차이가 없을 것입니다(RR 0.69, 95% CI 0.22 ~ 2.14; 1회 시험, 여성 1298명;분석 3.13). 비타민 D 그룹에서는 총 1039명 중 11명의 신생아 사망이 보고되었으며 무개입 또는 위약 그룹에서는 259명 중 4명의 신생아 사망이 보고되었습니다. 이 결과에 대한 데이터가 부족하기 때문에 확실한 결론을 내릴 수는 없습니다.
(4) 비타민 D + 칼슘 보충 대 칼슘(그러나 비타민 D는 없음)(시행 없음)
이 비교에는 임상시험이 포함되지 않았습니다.
(5) 비타민 D + 칼슘 + 기타 비타민 및 미네랄 보충 대 기타 비타민 및 미네랄(그러나 비타민 D + 칼슘은 없음)(시행 없음)
이 비교에는 임상시험이 포함되지 않았습니다.
논의
주요 결과 요약
이 검토에서는 임신 중 비타민 D 보충 단독 또는 칼슘, 기타 비타민 및 미네랄과의 조합의 효과를 평가합니다. 여기에는 7,033명의 여성을 대상으로 한 30건의 임상시험이 포함되어 있으며, 그 중 22건은 비타민 D 단독과 무치료 또는 위약을 비교했고, 9건은 비타민 D와 칼슘을 중재하지 않은 것과 비교했으며, 1건은 비타민 D와 칼슘, 철, 엽산을 비타민 D 없음과 비교했습니다. 비타민 D + 칼슘 + 기타 비타민 및 미네랄의 효과를 다른 비타민 및 미네랄과 비교하여 평가한 임상시험은 없습니다(그러나 비타민 D + 칼슘은 제외).
중재가 없거나 위약과 비교하여 비타민 D 보충.
-
아마도 자간전증 위험(4건의 임상시험), 임신성 당뇨병 위험(4건의 임상시험), 저체중아(2500g 미만) 출산 위험(5건의 임상시험)을 줄일 수 있을 것입니다.
-
조산 위험에 거의 또는 전혀 차이가 없을 수 있습니다(7건의 임상시험).
-
산모의 부작용 측면에서, 비타민 D 보충은 심각한 산후 출혈의 위험을 줄일 수 있습니다. 그러나 이 결과는 단일 임상시험의 결과에 기초한 것이며 이전에 다른 연구에서 문서화되지 않은 예상치 못한 결과라는 점에 유의해야 합니다. . 신증후군 위험에 미치는 영향은 불확실합니다. 어떤 임상시험에서도 고칼슘혈증 사례가 보고되지 않았습니다. 그러나 산모의 이상반응에 대한 일반적인 데이터가 부족하기 때문에 확고한 결론을 내릴 수는 없습니다.
2차 결과의 경우, 중재가 없거나 위약에 비해 비타민 D를 보충하면 아마도 25‐하이드록시비타민 D 농도가 더 높아질 것입니다(14개 시험). 보충에 대한 반응은 매우 이질적이므로 이 결과는 조심스럽게 해석되어야 합니다. 이는 시험에 사용된 다양한 용량(200 IU/일 ~ 4000 IU/일 범위), 다양한 보충 빈도(예: 매일, 매주 또는 볼루스), 다양한 보충 시작(예: 이전 또는 이전) 때문일 수 있습니다. 20주 후), 그리고 혈청 25‐하이드록시비타민 D를 평가하는 방법의 차이도 있습니다. 이 바이오마커는 어렵고 복잡하며 사용된 방법 간에 결과의 변동성이 높습니다( Holick 2008 ). 고성능 액체 크로마토그래피 질량 분석법이 가장 좋은 방법이지만( Holick 2005 ), 단 두 번의 시도에서만 이 방법을 사용했습니다. 따라서 결과를 주의해서 해석해야 합니다.
중재가 없거나 위약과 비교하여 비타민 D + 칼슘 보충.
-
아마도 전자간증의 위험을 줄일 수 있습니다(4건의 임상시험).
-
37주 미만에 조산 위험이 증가할 수 있습니다(5건의 임상시험). 그러나 결과는 주로 단 하나의 시험에 의해서만 결정됩니다. 그러므로 결과는 주의해서 해석되어야 합니다.
-
임신성 당뇨병 위험(1건의 임상시험)과 저체중아 출산 위험(2건의 임상시험)에 미치는 영향이 불확실합니다.
-
산모의 부작용에 대해 보고된 임상시험은 없습니다.
1건의 시험에서만 비타민 D, 칼슘, 철, 엽산의 보충을 칼슘, 철, 엽산과 비교하여 평가했지만 비타민 D는 평가하지 않았으며 조산이나 저체중아 출산 위험에 거의 또는 전혀 차이가 없었으며 기타 결과에 대한 결과는 불분명했습니다. 근거의 확실성이 매우 낮기 때문입니다.
일반적으로 산모의 이상반응 위험에 대해 결론을 내리려면 더 많은 데이터가 필요합니다.
증거의 전반적인 완전성과 적용 가능성
본 검토의 목적은 임신 및 신생아 결과 개선을 위한 위약 또는 무중재와 비교하여 임신 중 비타민 D 보충제의 모든 용량을 제공하는 임상시험을 비교하는 것이었습니다. 이번 업데이트에는 포함된 임상시험 수가 이전 버전( De‐Regil 2016 ) 에 비해 두 배로 늘어났 으며 일부 결과는 더욱 일관성이 있는 것으로 보입니다. 그러나 특정 산모 결과(부작용, 내당능 장애, 임신성 고혈압 또는 사망)와 영아 결과(신생아 사망, 신생아기에 특별 관리 입원, Apgar 점수가 낮음)를 보고하는 임상시험의 수가 여전히 제한되어 있습니다. 5분에 7시 이상, 신생아 감염 또는 조기 출산).
일반적으로 이 검토에서는 비타민 D 보충이 자간전증과 임신성 당뇨병의 위험을 줄이고 저체중 출생의 위험을 줄일 수 있지만 조산의 위험에는 거의 또는 전혀 차이가 없을 수 있음을 보여주었습니다. 개입의 안전성을 결정하려면 더 많은 정보가 필요합니다.
개요에서 누락된 내용은 무엇입니까?
대부분의 결과는 소수의 시험(2~5회 시험)과 더 큰 표본 크기에서만 보고되었기 때문에 각 주요 결과에 대해 더 많은 시험이 필요합니다. 대부분의 임상시험은 100명 미만의 참가자를 포함한 14개의 임상시험으로 중소 규모였습니다( Asemi 2012 , Asemi 2013a , Benson 2009 , Bhutta 2011 , Delvin 1986 , Diogenes 2013 , Kaur 1991 , Li 2000a , Mallet 1986 , Mazurkevich 2013 , Sabet 2012 ) . ; Samimi 2016 ; Samimi 2017 ; Shahgheibi 2016 ), 참가자 100~500명을 포함한 13건의 임상시험( Brooke 1980 ; Grant 2013 ; Marya 1987 ; Marya 1988 ; Mirghafourvand 2013 ; Naghshineh 2016 ; Roth 2010 ; Sablok 2015 ; 사산 2017 ; 싱 2015 ; 테흐 라니 2014 ; Vaziri 2016 ; Yu 2008 ), 500명 이상의 참가자가 포함된 단 3개의 임상시험( Harvey 2012 ; Roth 2013 ; Taherian 2002 ). 또 다른 누락 요인은 비타민 D 상태의 두 가지 중요한 결정 요인인 임신 전 체질량 지수(BMI)와 피부 색소 침착을 지정하지 않았다는 것입니다. 또한 대부분의 임상시험에서는 임상시험 시작 시 비타민 D 상태를 고려하지 않았습니다. 비타민 D 보충제의 효과는 비타민 D 결핍증이 있는 여성에게 더욱 심할 수 있으므로 이는 중요합니다. 대부분의 임상시험에서는 비타민 D를 단독으로 또는 칼슘과 함께 제공했습니다. 단 한 번의 시험( Roth 2013 )만이 비타민 D를 실제로 대부분의 여성이 섭취하는 다른 영양소와 비교했습니다. 테스트해야 하는 식이보충제의 영양소 간에 상호 작용이 있을 수 있으므로 이를 평가하는 것이 중요합니다. 또한 20주차 이전에 보충을 시작한 시험은 7개에 불과하므로 임신 초기부터 더 많은 시험이 필요합니다( Benson 2009 ; Bhutta 2011 ; Harvey 2012 ; Naghshineh 2016 ; Samimi 2017 ; Singh 2015 ; Tehrani 2014 ). 1,25 디히드록시 비타민 D3의 합성을 촉매하는 효소 1-알파-수산화효소가 임신 초기에 가장 높은 수준으로 발현되고 감소되기 때문에 임신 초기에 시작하면 비타민 D의 효과가 더 중요할 수 있습니다. 임신 3분기로 접어들면서 임신 초기에 가능한 역할을 강조합니다(젠더 2002 ).
따라서 임신 초기에 시작하여 비타민 D와 다른 영양소의 조합이 산모 및 유아 결과에 미치는 영향을 테스트하는 대규모 시험이 필요합니다. 또한 이러한 임상시험에서는 임신 전 BMI, 피부 색소 침착, 비타민 D 상태를 기본적으로 고려해야 합니다. 비타민 D가 부족한 사람이 더 많은 혜택을 받을 수 있기 때문입니다. Roth 2013 의 시험은 지금까지 최대 규모(참가자 1,500명 이상)였으며 비타민 D 결핍이 64%인 여성을 대상으로 다른 영양소와 함께 다양한 비타민 D 용량을 테스트했지만 임신 중반에 시작되었습니다. 이는 이러한 건강 결과에 중요한 영향이 없다는 것을 설명할 수 있습니다. 앞서 언급한 바와 같이, 1-알파-수산화효소는 임신 초기에 가장 높은 수준으로 발현되며, 이는 임신 초기에 그 역할이 가능함을 강조합니다( Zehnder 2002 ).
제외된 60건의 임상시험을 확인했는데, 그 이유는 주로 위약이나 보충제 없이 다양한 용량의 비타민 D를 비교했거나 포도당 불내성, 임신성 당뇨병 또는 기타 만성 질환이 있는 임산부를 대상으로 실시했기 때문입니다. 대부분의 국가에서는 산전 보충 지침에 비타민 D를 포함시키는 정책이 없기 때문에 다양한 복용량과 위약이 없는 임상시험은 포함하지 않았습니다. 그러므로 먼저 비타민 D 보충이 위약군이나 무개입군에 비해 유익한지 판단하는 것이 중요합니다.
우리가 아는 한, 현재 6개의 임상시험이 진행 중이며, 일단 발표되면 이 업데이트된 검토를 위해 확인된 증거의 규모가 더욱 늘어날 것입니다. 또한 업데이트에는 중요한 임신 결과에 대한 비타민 D 보충의 용량 반응이 포함될 수 있습니다. 실제로, 산전 및 신생아 건강 결과 개선을 위해 임신 중에 제공할 수 있는 최상의 요법을 결정하기 위해 다양한 용량의 비타민 D를 사용한 실험을 고려하는 또 다른 검토가 있습니다( Palacios 2018 ).
증거의 질
14건의 임상시험에서는 할당 및/또는 눈가림의 경우, 10건의 임상시험에서는 탈퇴의 경우 비뚤림 위험이 높았습니다. 또한 결과는 시험마다 상당히 달랐으며 이는 사용된 비타민 D 요법의 다양성과 관련이 있을 수 있습니다. 예를 들어, 9번의 임상시험에서는 하루에 약 200~600IU의 비타민 D를 사용했습니다. 이는 낮은 복용량으로 간주될 수 있지만 여러 조직에서 임신에 권장하는 복용량입니다( EFSA 2016 ; IOM 2011 ; RCOG 2014 ; WHO 2004 ). 12개 연구에서는 하루에 800~2000IU의 중간 용량의 비타민 D를 사용했습니다. 8건의 임상시험에서는 하루에 2000IU 이상의 비타민 D를 사용했습니다. 또한 매일 비타민 D를 제공하는 20건의 임상시험으로 보충 빈도에도 큰 변동이 있었습니다. 매주 또는 매월 6회; 3개는 1~2회 볼루스 용량을 투여했고, 1개는 매일 결합하여 볼루스를 투여했습니다. 마지막으로, 앞서 언급한 바와 같이, 20주차 이전에 보충을 시작한 임상시험은 7건뿐입니다. 비타민 D의 효과는 1,25 디하이드록시 비타민 D3의 합성을 촉매하는 효소 1-알파-수산화효소로서 임신 초기에 시작하는 경우 더 중요할 수 있습니다. , 첫 번째 삼 분기에 가장 높은 수준의 발현을 가지며 세 번째 삼 분기로 갈수록 감소하여 임신 초기에 가능한 역할을 강조합니다( Zehnder 2002 ). 이러한 차이는 관찰된 결과에 영향을 미쳤을 수 있습니다.
비뚤림 위험과 연구 결과를 기반으로 비교 1(비타민 D 단독 대 위약/무개입;1 번 테이블), 비교 2(비타민 D + 칼슘 대 위약/무개입;표 2) 및 비교 3(비타민 D + 칼슘 + 기타 비타민 및 미네랄 대 칼슘 + 기타 비타민 및 미네랄, 비타민 D 없음;표 3). 불일치나 출판 편향이 있을 가능성은 없다고 생각했지만, 시험의 편향 위험과 부정확성으로 인해 자간전증, 임신성 당뇨병, 저체중 출생에 대한 중간 정도 확실성의 증거가 나타났습니다. 심각한 산후 출혈, 고칼슘혈증 및 조산에 대한 낮은 확실성의 증거; 비타민 D 단독 보충과 중재 없음 또는 위약 비교에서 신증후군에 대한 확실성이 매우 낮다는 증거가 있습니다. 비타민 D와 칼슘의 보충을 평가하는 임상시험에서 근거의 확실성은 자간전증의 경우 중간 수준이었고 조산의 경우 낮았으며 임신성 당뇨병 및 저체중 출생의 경우 매우 낮았습니다. 비타민 D + 칼슘 + 기타 비타민 및 미네랄의 보충을 평가하는 임상시험의 근거 확실성은 조산 및 저체중아 출산에 대해서는 낮았고, 임신성 당뇨병 및 산모 부작용에 대해서는 매우 낮았습니다.
검토 과정의 잠재적 편견
우리는 검토 과정에서 몇 가지 잠재적인 편견을 확인했습니다. 이는 두 가지 방법으로 최소화되었습니다. (1) 두 명의 검토 저자가 포함 및 데이터 추출에 대한 적격성을 독립적으로 평가했으며 (2) 비뚤림 위험 및 데이터 입력에 대한 평가도 두 명의 검토 저자가 독립적으로 평가했습니다. 그러나 적격성과 비뚤림 위험에 대한 평가를 검토할 때 여러 가지 주관적인 판단이 필요합니다. 다른 사람들은 이러한 문제에 관해 다른 결정을 내릴 수도 있습니다. 결과 해석에 도움이 되도록 독자들이 포함된 연구의 특성 표 를 검토하도록 권장합니다 .
다른 연구 또는 리뷰와의 동의 및 불일치
이 리뷰는 임신 중 비타민 D 보충에 관한 이전 Cochrane 리뷰를 업데이트합니다( De‐Regil 2012 ; De‐Regil 2016 ). 2012년 검토에는 총 1023명의 여성을 대상으로 한 6개의 시험이 포함되었고 8개의 시험은 제외되었으며 6개의 시험은 여전히 진행 중이었습니다. 2016년 검토에는 총 2,833명의 여성을 평가한 15개의 시험이 포함되었고 27개의 시험은 제외되었으며 23개의 시험은 아직 진행 중이거나 출판되지 않았습니다. 2016년 검토에서 저자는 임산부에게 비타민 D를 보충하면 만삭 시 혈청 25‐하이드록시비타민 D가 크게 증가하고 전자간증, 저체중아 출산 및 조산의 위험을 줄일 수 있다고 결론지었습니다. 그러나 비타민D와 칼슘이 결합되면 조산 위험이 높아질 수 있습니다. 이번 업데이트의 결과는 유사하지만 각 결과에 대해 보고된 임상시험의 수가 많아짐에 따라 더욱 강화되었습니다. 언급된 유일한 차이점은 2016년 검토에서는 임신 중에 비타민 D를 보충한 여성에게서 태어난 영아의 머리 둘레가 더 높은 것으로 나타났으나 이번 업데이트에서는 이것이 관찰되지 않았다는 것입니다. 다른 산모 및 유아 건강 결과에 대한 영향을 확인하기에는 아직 데이터가 충분하지 않습니다. 이는 단 한두 번의 임상시험에서만 보고되거나 평가되지 않았기 때문입니다.
우리의 결과는 다른 유사한 체계적인 검토와 부분적으로 일치합니다. 예를 들어, Harvey 2014에서는 비타민 D 보충과 위약 또는 낮은 수준의 비타민 D가 산모 및 신생아 건강 결과에 미치는 영향을 비교했습니다. 출생 체중을 평가한 7건의 임상시험 중 3건의 임상시험에서는 영양보충을 받은 산모의 영아에서 출생시 체중이 유의미하게 증가한 것으로 나타났으나 나머지 4건에서는 유의미한 효과가 발견되지 않았습니다. 출생 기간에 대해서는 두 가지 시험이 확인되었습니다. 한 연구에서는 비타민 D를 보충하면 보충을 받은 여성의 영아의 출생 기간이 길어진다는 사실을 발견했고, 다른 연구에서는 대조군에 비해 "유의한 연관성은 없지만 보충 그룹에서 출생 기간이 길어지는 추세"라는 인용문을 발견했습니다. 또한, 새끼의 머리 둘레를 평가한 두 가지 시험에서 하나는 보충된 어미의 머리 둘레가 유의미하게 더 큰 것으로 나타났고, 다른 하나는 보충된 어미의 머리 둘레가 더 큰 경향을 발견했습니다. 자간전증에 대한 중재는 하나만 확인되었으며(그룹 간 위험 차이는 없음) 조산, 저체중 출생, 임신성 당뇨병 및 제왕절개에 대한 중재는 확인되지 않았습니다. 13개 시험(n = 2299)에 대한 또 다른 체계적 검토 및 메타 분석에서는 비타민 D 보충(칼슘 포함 또는 제외)을 임신 중 낮은 수준의 비타민 D(400 IU/일)를 포함하는 위약 그룹과 비교했습니다( Perez‐ 로페즈 2015 ). 만기 혈청 25‐하이드록시비타민 D는 대조군에 비해 비타민 D가 높은 그룹에서 유의하게 더 높았습니다(평균 차이: 66.5 nmol/L, 95% 신뢰 구간(CI) 66.2 ~ 66.7, 10건의 시험, 1468명의 참가자). 현재 리뷰. 그러나 현재 검토와는 달리 Perez‐Lopez 2015에서는 비타민 D 보충이 전자간증(3건의 임상시험, 654명의 참가자), 임신성 당뇨병(3건의 임상시험, 384명의 참가자), 저체중 출생(4건의 임상시험, 496명)에 영향을 미치지 않는 것으로 나타났습니다. 참가자) 및 조산(3건의 임상시험, 384명의 참가자), 출생 체중(10건의 임상시험, 1489명의 참가자) 및 출생 기간(6건의 임상시험, 866명의 참가자)이 유의하게 증가했습니다. 현재 검토와 일치하게 비타민 D 보충은 제왕절개에 영향을 미치지 않았습니다(4건의 임상시험, 1028명의 참가자). 또 다른 검토에서는 자간전증 위험을 줄이기 위해 낮은 비타민 D 용량(400 IU/일) 또는 임신 중 개입 없음을 포함하는 대조군과 비교하여 비타민 D 보충의 효과를 평가했습니다( Hyppönen 2013). 5,871명의 여성을 포함하여 확인된 4개의 임상시험 중 2개의 연구에서는 2000IU/일과 4000IU/일을 비교했고, 또 다른 연구에서는 1200IU/일과 비타민 D 없음을 비교했으며, 매우 오래된 임상시험에서는 450IU/일과 비타민 D 없음을 비교했습니다. 시험에서는 여러 보충제를 보충제가 없는 것과 비교했습니다. 그들은 중재가 대조군에 비해 자간전증의 위험을 크게 감소시키는 것으로 나타났습니다(교차비(OR) 0.66; 95% 신뢰 구간(CI) 0.52~0.83). 그러나 그들은 매우 다른 시험을 사용했습니다. Thorne‐Lyman 2012 의 검토에는 위약 또는 대조군을 대상으로 저용량 비타민 D(400IU/일)를 사용한 시험도 포함되었습니다. 비타민 D 보충이 포함된 2건의 임상시험(참가자 529명)에서는 조산 감소 효과가 관찰되지 않았습니다. 그러나 보충제를 사용하면 저체중 출생 위험이 60% 더 낮은 것으로 관찰되었습니다(3건의 임상시험, 507명의 참가자). 총 8,406명의 참가자가 포함된 43건의 임상시험을 포함한 Roth 2017 의 보다 최근의 체계적인 검토에서는 비타민 D 보충과 위약 그룹(600 IU/일 미만) 또는 중재 없음을 비교했습니다. 비타민 D 보충은 만삭 시 산모의 25‐하이드록시비타민 D를 유의하게 증가시켰지만 용량 반응 효과는 약했습니다. 또한, 비타민 D 보충에 배정된 여성은 대조군에 비해 평균 출생 체중이 더 높은 영아를 낳았지만, 우리의 검토와는 달리 자간전증, 임신성 당뇨병, 조산 및 저체중 출생 위험에 대한 영향은 발견되지 않았습니다. 그러나 이 리뷰와 유사하게 Roth 2017 에서는 비타민 D 보충이 임신성 고혈압, 제왕절개, 병원 입원, 신생아 사망, 사산 또는 기타 부작용의 위험에 미치는 영향을 발견하지 못했습니다. 이 메타 분석에서는 또한 대부분의 임상시험이 비뚤림 위험이 높다는 사실을 발견했습니다. Roth 2017에는 대조군에 비타민 D 수치가 낮은 임상시험이 포함된 반면, 대조군에는 비타민 D가 없거나 개입이 없는 임상시험만 포함되었다는 점에 유의하는 것이 중요합니다 .
전반적으로, 이용 가능한 체계적 검토와 메타 분석에서는 비타민 D 보충으로 혈청 25‐하이드록시비타민 D 수치가 크게 향상되는 것으로 일관되게 나타났습니다. 그러나 결과에는 중요한 차이가 있습니다. 이 리뷰와 다른 리뷰( Hyppönen 2013 )에서는 비타민 D 보충을 통해 자간전증 위험이 크게 감소한 것으로 나타났지만, 다른 두 리뷰( Perez‐Lopez 2015 ; Roth 2017 )에서는 이를 발견하지 못했습니다. 또한 조산, 임신성 당뇨병, 저체중아 출산 위험 감소에서도 차이가 발견되었습니다. 본 검토 결과와 앞서 언급한 검토 결과 사이에 발견된 주요 차이점은 시험의 포함 기준입니다. 우리는 비타민 D의 모든 용량을 0 IU/일 또는 중재가 없는 위약 그룹과 비교한 임상시험만 포함했습니다. 그러나 위에 설명된 임상시험에는 비타민 D 수치가 낮거나 중재가 없는 위약군과 비타민 D 보충을 비교하는 임상시험이 포함되었습니다.
안전성과 관련하여, 산모와 유아의 안전 관련 결과를 보고하는 임상시험에서는 비타민 D 보충제가 임신 중에 안전할 수 있음을 시사할 수 있습니다. 그러나 이는 출혈, 신증후군, 고칼슘혈증 및 고칼슘뇨증을 평가하는 등 임상시험에서 다르게 평가되었습니다. 따라서 이 개입의 안전성에 대해서는 여전히 추가 연구가 필요합니다. 또한 본 검토에서 정의된 대부분의 2차 결과(산모 사망, 신생아 중환자실 입원, 5분에 7 미만의 Apgar 점수, 신생아 감염 또는 조기 출산)는 어떤 임상시험에서도 보고되지 않았습니다. Sablok 2015 의 시험에서는 Apgar 점수가 3~7 미만으로 보고되었으며 보충제 그룹과 위약 그룹 간에 차이가 없었습니다. 확실한 결론을 내리기 위해 이러한 안전 관련 결과를 보고하려면 더 많은 시험이 필요합니다.
감사의 말
출판 전 편집 과정의 일환으로, 이 리뷰는 Cochrane Pregnancy and Childbirth의 국제 소비자 패널 구성원이자 그룹의 통계 고문인 두 명의 동료(편집팀 외부의 편집자 및 심판자)의 의견을 받았습니다. 저자들은 시간을 내어 의견을 주신 다음 동료 평가자에게 감사드립니다. Zulfiqar A Bhutta, Robert Harding 글로벌 아동 건강 및 정책 의장, 글로벌 아동 건강 센터, The Hospital for Sick Children, 토론토, 캐나다; 파키스탄 카라치 소재 아가 칸 대학교 여성 및 아동 건강 우수 센터 창립 이사입니다.
이 프로젝트는 Cochrane Pregnancy and Childbirth에 대한 Cochrane 인프라 자금 지원을 통해 국립 보건 연구소(National Institute for Health Research)의 지원을 받았습니다. 여기에 표현된 견해와 의견은 저자의 견해와 의견이며 체계적 검토 프로그램, NIHR, NHS 또는 보건부의 견해와 의견을 반드시 반영하는 것은 아닙니다.
세계보건기구(WHO), Cristina Palacios 및 Lia Kostiuk는 WHO가 수시로 수행할 수 있는 원고에 대한 수정 또는 업데이트를 포함하여 출판을 위해 제출된 이 업데이트된 리뷰 원고에 대한 저작권 및 기타 모든 권리를 보유합니다. 우리는 이 리뷰의 이전 버전에서 Luz‐Maria De‐Regil, Ali Ansary 및 Regina Kulier의 지원을 인정합니다.
Juan Pablo Peña‐Rosas는 현재 WHO의 직원입니다. 본 출판물에 표현된 견해에 대한 책임은 저자에게만 있으며 반드시 WHO의 결정, 정책 또는 견해를 대변하는 것은 아닙니다.
이 리뷰의 이전 버전에 저자로서 기여한 Kassam Mahomed에게 감사드립니다.
부록
부록 1. 추가 저자 검색에 사용되는 검색어
저자는 "비타민 D 보충 및 임신"이라는 용어를 사용하여 ClinicalTrials.gov 및 WHO가 주최하는 국제 임상 시험 등록 플랫폼(ICTRP)에서 진행 중이거나 계획된 시험(2018년 7월 12일)을 검색했습니다.
연구의 특징
프로토콜과 검토의 차이점
본 2019년 업데이트 리뷰 는 이전 버전( De‐Regil 2016 )과 비교하여 다음과 같은 차이점이 있습니다.
-
이 리뷰의 담당자(및 보증인)가 Luz Maria De‐Regil에서 Cristina Palacios로 변경되었습니다. 두 명의 이전 공동저자는 전체 검토 단계에서 검토팀을 떠났습니다.
저자의 기여
이번 업데이트에서 Lia Kostiuk와 Juan Pablo Peña‐Rosas는 새로운 임상시험의 적격성을 평가하고 데이터를 중복해서 추출했습니다. 모든 차이점은 Cristina Palacios와 논의하고 해결되었습니다. 모두 업데이트된 리뷰 준비에 기여했습니다.
 뼈 건강 및 골다공증에서 비타민 D 3 이상의 비타민의 역할 (검토)
뼈 건강 및 골다공증에서 비타민 D 3 이상의 비타민의 역할 (검토)